
| A. | 15种 | B. | 28种 | C. | 32种 | D. | 40种 |
分析 分子式为C5H10O2的酯为饱和一元酯,形成酯的羧酸与醇的碳原子总数为5,讨论羧酸与醇含有的碳原子,判断形成该酯的羧酸与醇的同分异构体种数,根据羧酸与醇组合,计算同分异构体数目.
解答 解:分子式为C5H10O2的有机物在酸性条件下可水解为酸和醇,属于饱和一元酯,
若为甲酸和丁醇酯化,甲酸只有1种,丁醇有4种;
若为乙酸和丙醇酯化,乙酸只有1种,丙醇有2种;
若为丙酸和乙醇酯化,丙酸只有1种,乙醇只有1种;
若为丁酸和甲醇酯化,丁酸有2种,甲醇只有1种;
故羧酸共有5种,醇共有8种,酸和醇重新组合可形成的酯共有5×8=40种,
故选D.
点评 本题考查同分异构体的书写与判断,难度中等,关键是形成酯的羧酸与醇的同分异构体的判断,注意利用数学法进行计算.


 精英口算卡系列答案
精英口算卡系列答案科目:高中化学 来源: 题型:解答题
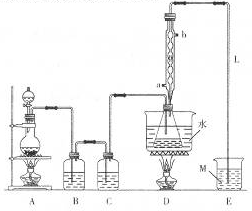 S2Cl2是工业上常用的硫化剂,广泛应用于石油化工.实验室制备S2Cl2的方法有两种:
S2Cl2是工业上常用的硫化剂,广泛应用于石油化工.实验室制备S2Cl2的方法有两种:| S | CS2 | CCl4 | S2Cl2 | |
| 熔点/ | 113 | -109 | -23 | -77 |
| 沸点/ | 445 | 47 | 77 | 137 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

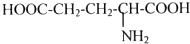 (写结构简式)可以合成二肽(如图2)
(写结构简式)可以合成二肽(如图2)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入SO3 | B. | 压强不变,充入Ar | C. | 容积不变,充入Ar | D. | 降低温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
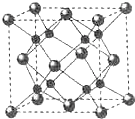 A、B、C、D为原子序数依次增大的四种元索,A2-和B+具有相同的电子构型;C、D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题:
A、B、C、D为原子序数依次增大的四种元索,A2-和B+具有相同的电子构型;C、D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上用石灰乳与氯气制漂白粉 | B. | 工业上电解熔融状态Al2O3制备Al | ||
| C. | 工业上利用合成氨实现人工固氮 | D. | 自来水厂用明矾做净水剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ③② | C. | ③① | D. | ①②③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com