
在反应X+2Y═R+M中,已知R和M的摩尔质量之比为22:9,当1.6gX与Y完全反应后,生成4.4gR,则此反应中Y和M的质量之比为()
| A. | 16:9 | B. | 32:9 | C. | 23:9 | D. | 46:9 |
科目:高中化学 来源: 题型:
按如图所示装置进行实验,并回答下列问题:
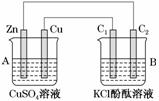 (1)判断装置的名称:A池为________,B池为________________。
(1)判断装置的名称:A池为________,B池为________________。
(2)锌极为________极,电极反应式为__________________;
铜极为________极,电极反应式为________________________________________
________________________________________________________________________;
石墨棒C1为____极,电极反应式为______________________________________
________________________________________________________________________;
石墨棒C2附近发生的实验现象为________________________________________
________________________________________________________________________。
(3)当C2极析出224 mL气体(标准状况)时,锌的质量________(填“增加”或“减少”)________g,CuSO4溶液的质量________(填“增加”或“减少”)________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知常温下反应,①NH3+H+NH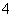 (平衡常数为K1),②Ag++Cl-AgCl(平衡常数为K2),③Ag++2NH3Ag(NH3)
(平衡常数为K1),②Ag++Cl-AgCl(平衡常数为K2),③Ag++2NH3Ag(NH3)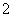 (平衡常数为K3)。①、②、③的平衡常数关系为K1>K3>K2,据此所做的以下推测合理的是( )
(平衡常数为K3)。①、②、③的平衡常数关系为K1>K3>K2,据此所做的以下推测合理的是( )
A.氯化银不溶于氨水
B.银氨溶液中加入少量氯化钠有白色沉淀
C.银氨溶液中加入盐酸有白色沉淀
D.银氨溶液可在酸性条件下稳定存在
查看答案和解析>>
科目:高中化学 来源: 题型:
化学反应原理在科研和生产中有广泛应用。
(1)利用“化学蒸气转移法”制备TaS2晶体,发生如下反应:
TaS2(s)+2I2(g)TaI4(g)+S2(g) ΔH>0 (Ⅰ)
反应(Ⅰ)的平衡常数表达式K=________,若K=1,向某恒容容器中加入1 mol I2(g)和足量TaS2(s),I2(g)的平衡转化率为________。
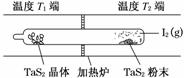
(2)如图所示,反应(Ⅰ)在石英真空管中进行,先在温度为T2的一端放入未提纯的TaS2粉末和少量I2(g),一段时间后,在温度为T1的一端得到了纯净TaS2晶体,则温度T1________T2(填“>”“<”或“=”)。上述反应体系中循环使用的物质是________。
(3)利用I2的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,所用指示剂为________,滴定反应的离子方程式为
________________________________________________________________________
________________________________________________________________________。
(4)25 ℃时,H2SO3HSO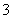 +H+的电离常数Ka=1×10-2mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kh=________mol·L-1,若向NaHSO3溶液中加入少量的I2,则溶液中
+H+的电离常数Ka=1×10-2mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kh=________mol·L-1,若向NaHSO3溶液中加入少量的I2,则溶液中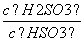 将________(填“增大”“减小”或“不变”)。
将________(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C三种物质各15g,发生如下反应:A+B+C→D反应后生成D的质量为30g.然后在残留物中加入10g A,反应又继续进行,待反应再次停止,反应物中只剩余C,则下列说法正确的是()
| A. | 第一次反应停止时,剩余B 9 g | |
| B. | 第一次反应停止时,剩余C 6 g | |
| C. | 反应中A和C的质量比是5:3 | |
| D. | 第二次反应后,C剩余5 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生用托盘天平称量时,误将药品与砝码的位置放颠倒了,待平衡时,称得药品质量的读数为9.5g(1g以下用游码),则药品的实际质量为()
| A. | 9g | B. | 10g | C. | 8.5g | D. | 8g |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列电离方程式中,错误的是()
| A. | H2CO3⇌H++HCO3﹣、HCO3﹣⇌H++CO32﹣ | |
| B. | H2SO4⇌2H++SO42﹣ | |
| C. | NaHCO3═Na++H++CO32﹣ | |
| D. | NaHSO4═Na++H++SO42﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是
A.近期媒体报道的某白酒中添加的塑化剂是对人体健康无害的物质
B.尽量使用含12C的产品,减少使用含13C或14C的产品符合“低碳经济”宗旨
C.大量二氧化碳气体的排放是形成酸雨的主要原因
D.使用太阳能、风能、潮汐能等能源能减少PM2.5的污染
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com