
【题目】(1)请正确表示下列化学用语:
乙炔(结构式) ;甲烷(空间构型) ;羟基(电子式) ;
C22-(电子式) _________ ;1,3-丁二烯(实验式) 。
(2)高分子化合物![]() 是由三种单体通过加聚反应而制得的。这三种单体的结构简式是 、 、 ;
是由三种单体通过加聚反应而制得的。这三种单体的结构简式是 、 、 ;
(3)提纯下列物质(括号内为杂质)
①NaCl(KNO3)固体中提取NaCl固体: 。
②KNO3(NaCl)溶液中得KNO3固体: 。
③乙醇(水)混合物中得无水乙醇: 。
④溴苯(溴)混合物中得溴苯: 。
【答案】(1)![]() ;正四面体形;
;正四面体形;![]() ;
;![]() ;C2H3。
;C2H3。
(2) CH2=C(CH3)—CH=CH、CH3—CH=CH2、CH2=CH2
(3)①加水溶解,蒸发结晶,趁热过滤 ②蒸发浓缩,冷却结晶,过滤 ③加入CaO,再蒸馏 ④加入NaOH溶液,再分液
【解析】
试题分析:(1)乙炔的结构式为![]() ;甲烷的空间构型为正四面体形;羟基的电子式为
;甲烷的空间构型为正四面体形;羟基的电子式为![]() ;C22-的电子式为
;C22-的电子式为![]() ;1,3-丁二烯的实验式为C2H3。
;1,3-丁二烯的实验式为C2H3。
(2)![]() 的三种单体分别是 CH2=C(CH3)—CH=CH、CH3—CH=CH2、CH2=CH2 ;
的三种单体分别是 CH2=C(CH3)—CH=CH、CH3—CH=CH2、CH2=CH2 ;
(3)①NaCl(KNO3)固体中提取NaCl固体应加水溶解,蒸发结晶,趁热过滤。②KNO3(NaCl)溶液中得KNO3固体应蒸发浓缩,冷却结晶,过滤。③乙醇(水)混合物中得无水乙醇加入CaO,再蒸馏。④溴苯(溴)混合物中得溴苯加入NaOH溶液,再分液。


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】有一位厨师不小心把刚熬好的羊油碰翻在灶坑旁,与草木灰混在一起,当他将羊油与草木灰的混合物用手捧出去后,洗手时发现手洗得特别干净。对此下列解释正确的是
A.羊油是一种有机溶剂,溶解了厨师手上的油污
B.草木灰呈碱性,与羊油发生了中和反应,除去油污
C.羊油与草木灰中的物质发生了加成反应,除去油污
D.羊油在碱性草木灰(主要成分为K2CO3)的作用下发生了皂化反应,生成具有去油污能力的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修化学与技术】铝是一种重要的金属,在生产、生活中具有许多重要的用途,如下框图是从铝土矿中制备铝的工艺流程:

已知:①铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质;
②溶液中的硅酸钠与偏铝酸钠反应,能生成硅铝酸盐沉淀,化学方程式为:2Na2SiO3+2NaAlO2+4H2O=Na2Al2Si2O8↓+2H2O+4NaOH
回答下列问题:
(1)溶解铝土矿时,发生反应的离子方程式为:____________。
(2)滤渣A的主要成分________;硅铝酸盐沉淀写成氧化物的形式是________。
(3)在工艺流程第三步中,选用二氧化碳作酸化剂而不使用盐酸的原因是 _。
(4)若该工厂用![]() kg铝土矿共制得
kg铝土矿共制得![]() kg Al(假设每步反应进行完全),则铝土矿中Al2O3的质量分数为______。
kg Al(假设每步反应进行完全),则铝土矿中Al2O3的质量分数为______。
(5)若将铝溶解,下列试剂中最好选用_____ __(填编号)。
A.浓硫酸B. 稀硫酸C.稀HNO3 D.浓HNO3
(6)电解冶炼铝时用Na3AlF6作助熔剂, Na3AlF6是配合物,其中内界是___,配位数为_ ____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用LiOH可制备锂离子电池正极材料。LiOH可由电解法制备,如右图,两极区电解质溶液分别为LiOH和LiCl溶液。下列说法错误的是

A.B极区电解质溶液为LiOH溶液
B.阳极电极反应式为2Cl--2e-=Cl2↑
C.电解过程中主要是H+通过阳离子交换膜向B电极迁移
D.电极A连接电源的正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。请推断后回答下列问题:
(1)Z在Y单质中燃烧的产物电子式为
用电子式表示X与R化合物的形成过程
(2)Y、Z、W、R形成的简单离子半径由大到小顺序为
(3)W单质与Z的最高价氧化物对应的水化物反应的离子方程式为
W单质与R的最高价氧化物对应的水化物反应的化学方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某矿石含碳酸镁和石英,制备高纯硅和硅胶的工艺流程如下:

(1)“硅胶”冶常用作_______________ ,也可以用作__________的载体。 A 的结构式为________。
(2)制备粗硅的方程式为_______。
(3)操作I为_____________,操作Ⅱ为_______________,操作Ⅲ所用仪器有铁架台(带铁圈)、酒精灯、_______________等。
(4)操作Ⅲ,需要在氯化氢气流中加热脱水的原因是_______________。
(5)溶液G用E酸化的方程式为_______________。
(6)电解饱和的K溶液的离子方程式为____________,阳极电极方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源、环境与人类的生活和社会发展密切相关。低碳、环保,能源的综合利用是是当今的热门话题。英国蒂斯河畔斯托克顿市的“空气燃料合成公司冶竟真的发明出了一种将空气变成汽油的高科技技术,而美国科学家最早设计出以甲烷等碳氢化合物为燃料的新型电池,大大提高天然气的利用效率。据此,回答下列问题:
(1)“空气变汽油”这项科技解决环境问题的意义是_______________________;
(2)“空气变汽油”其原理可简化如下:

则:
①合成路线中,NaOH 和盐酸都可以循环利用,写出有关反应式______________________;
②转变过中,100g5%Na2CO3溶液,电解后,溶液浓度变为10%,则生成标准状况下的氢气多少升?
(3)天然气燃料电池最大的障碍是氧化反应不完全,产生________ (填写化学式)堵塞电极的气体通道,有人估计,完全避免这种副反应至少还需10年时间。
(4)以下是天然气燃料电池电解精炼铜的装置图:

则,①甲池反应的离子方程式为______________________;
②当乙池中某电极的质量增重12.8g 时,理论上甲池中消耗的CH4在标准状况下的体积为__________mL,甲池中溶液的pH约为__________(溶液的体积变化忽略不计);此时向甲池中加入1 L1.0×10-3mol/L的CaCl2溶液,则甲池中________(填“有”或“无”)沉淀生成[已知Ksp(CaCO3)=2.9×10-9]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用氟磷灰石[(Ca5(PO4)3F)]生产磷铵[(NH4)3PO4]并制取硫酸、联产水泥。其工艺流程如下图所示:
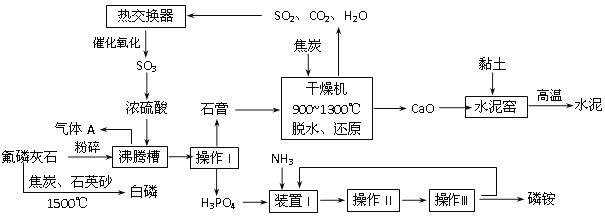
(1)操作I的名称________________;在实验室中操作II包括___________、____________。
(2)沸腾槽的材质是_______________(从“玻璃”、“钢铁”、“附有聚偏氟乙烯防腐层的石墨”中选择),选择的理由是__________________________________________________
(3)工业上还可以用氟磷灰石与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,同时逸出SiF4和CO,反应方程式为:_________________________________________。
(4)黏土中有一种成分为石脂(Al2[OH]4Si2O5·nH2O),其用氧化物表示为____________。
(5)已知SO2的催化氧化反应为2SO2(g)十O2(g) ![]() 2SO3(g) △H<0。
2SO3(g) △H<0。
从化学反应原理的角度说明催化氧化时使用热交换器的原因__________________。
(6)制硫酸所产生的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾。拟用下图所示的装置测定硫酸尾气中SO2的含量:

若下列各组中的试剂,前者浓度为0.1mol·L-1,后者适量,溶液体积为5mL;通入尾气10L(已换算为标准状况)时反应管中的溶液恰好变色。判断下列试剂组能否测定硫酸尾气中SO2的体积分数。能者,确定SO2的体积分数;不能者,说明原因。
编号 | 试剂组 | 结论 |
① | NaOH溶液、酚酞试液 | |
② | Na2CO3溶液、酚酞试液 | |
③ | 碘水、淀粉溶液 | |
④ | KMnO4溶液、稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸亚铬水合物{[Cr(CH3COO)2]22H2O,相对分子质量为376}是一种深红色晶体,不溶于冷水,是常用的氧气吸收剂.实验室中以锌粒、三氯化铬溶液、醋酸钠溶液和盐酸为主要原料制备醋酸亚铬水合物,其装置如右图所示,且仪器2中预先加入锌粒.已知二价铬不稳定,极易被氧气氧化,不与锌反应.制备过程中发生的相关反应如下:

Zn(s)+2HCl(aq)═ZnCl2(aq)+H2(g)
2CrCl3(aq)+Zn(s)═2CrCl2(aq)+ZnCl2(aq)
2Cr2+(aq)+4CH3COO-(aq)+2H2O(l)═[Cr(CH3COO)2]22H2O(s)
请回答下列问题:
(1)仪器1的名称是_____________。
(2)往仪器2中加盐酸和三氯化铬溶液的顺序最好是_____________(选下面的A、B或C);目的是_____________。
A.盐酸和三氯化铬溶液同时加入
B.先加三氯化铬溶液一段时间后再加盐酸
C.先加盐酸一段时间后再加三氯化铬溶液
(3)为使生成的CrCl2溶液与CH3COONa溶液顺利混合,应关闭阀门_____________(填“A”或“B”,下同),打开阀门_____________。
(4)本实验中锌粒要过量,其原因除了让产生的H2将CrCl2溶液压入装置3与CH3COONa溶液反应外,另一个作用是_____________。
(5)已知其它反应物足量,实验时取用的CrCl3溶液中含溶质9.51g,取用的醋酸钠溶液为1.5L0.1mol/L;实验后得干燥纯净的[Cr(CH3COO)2]22H2O9.4g,则该实验所得产品的产率为_____________(不考虑溶解的醋酸亚铬水合物)。
(6)铬的离子会污染水,常温下要除去上述实验中多余的Cr2+,最好往废液中通入足量的_____________,再加入碱液,调节pH至少为_____________才能使铬的离子沉淀完全(铬的离子浓度应小于10-5mol/L).已知Cr(OH)3的溶度积为6.3×10-31,![]() ≈4,lg2≈0.3
≈4,lg2≈0.3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com