
| A. | NaCl晶体、BaSO4 | B. | 铜、二氧化硫 | C. | 液态的HCl、酒精 | D. | KNO3溶液、CO2 |
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源:2016-2017学年山西省高一上期中化学试卷(解析版) 题型:选择题
如果你家里的食用花生油混有水份,你将采用下列何种方法分离
A.过滤 B.蒸馏 C.分液 D.萃取
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 标况下1molCCl4所占体积约为22.4L | |
| B. | 不同分散系其对应分散质的微粒直径不同 | |
| C. | 1molO2与1molO3所含的原子数目相等 | |
| D. | NaCl晶体和熔化的NaCl都属于电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

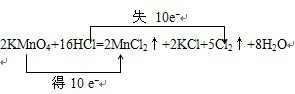
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al易导电,属于电解质 | |
| B. | BaSO4难溶于水,属于非电解质 | |
| C. | HCl的气体和液体都不导电,但HCl属于电解质 | |
| D. | SO2溶于水能导电,所以SO2是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
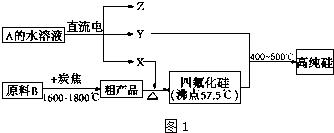
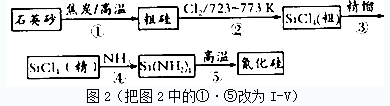
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com