
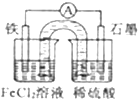
 某原电池装置如图所示,盐桥中装有用饱和氯化钾溶液浸泡过的琼脂.原电池工作一段时间后,下列叙述正确的是( )
某原电池装置如图所示,盐桥中装有用饱和氯化钾溶液浸泡过的琼脂.原电池工作一段时间后,下列叙述正确的是( )| A、FeCl2溶液中c(Cl-)会增大 |
| B、原电池装置中的盐桥完全可用金属导线代替 |
| C、铁电极上发生了氧化反应,右边溶液的pH减少 |
| D、电子由Fe电极经导线流向石墨电极,再经稀硫酸、盐桥、FeCl2溶液流回Fe电极 |


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔是物质的质量单位 |
| B、氢气的摩尔质量是2g |
| C、1mol H3O+ 的质量是19g |
| D、气体摩尔体积是指单位物质的量的物质所占的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaOH |
| B、KOH |
| C、CaO |
| D、Na2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X2Y的沸点比X2R高,是因为X2Y分子之间氢键比X2R分子之间的氢键强 |
| B、W与Y形成化合物的分子式为WY2 |
| C、WX4空间构型为正四面体形,WX4分子的稳定性强于甲烷 |
| D、原子半径按Z、W、R、Y、X的顺序依次减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、白酒 | B、白糖 | C、食醋 | D、纯碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入少量氢氧化钠 |
| B、加入少量盐酸 |
| C、加入少量水 |
| D、加热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com