
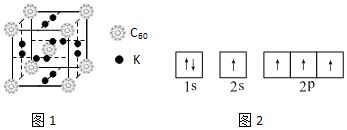
分析 (1)利用均摊法确定K原子和C60分子的个数比;
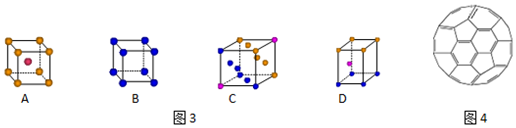
(2)根据能量最低原理可知,电子排布时优先占据能量低的轨道;
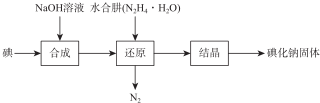
(3)钾是体心立方堆积,其配位数是8;
(4)①利用均摊法计算一个碳原子含有的σ键个数,在计算1mol C60分子中σ键的数目;
②物质的熔点与晶体类型有关,原子晶体的熔点大于分子晶体.
解答 解:(1)该晶胞中C60个数=1+8×$\frac{1}{8}$=2,6×2×$\frac{1}{2}$=6,所以K原子和C60分子的个数比为6:2=3:1,则化学式为K3C60;故答案为:K3C60;
(2)根据能量最低原理可知,电子排布时优先占据能量低的轨道,先排2s轨道后再排2p轨道,所以其轨道排布图违反了能量最低原理,其电子排布图为: ,
,
故答案为:能量最低原理;
(3)钾是体心立方堆积,其配位数是8,故答案为:A;8;
(4)①1个 C60分子中的一个碳原子含有1.5个σ键,所以一个 C60分子中含有90个σ键,则1mol C60分子中σ键的数目为90NA,
故答案为:90NA;
②原子晶体的熔点大于分子晶体,金刚石是原子晶体,C60是分子晶体,物质的熔点与键长无关,所以该说法错误,故答案为:错误,因为金刚石是原子晶体,而C60是分子晶体.
点评 本题考查了物质结构和性质,涉及晶胞的计算、电子排布图等知识点,难度不大,离子配位数的判断是学习难点,会运用均摊法计算化学键、晶胞的化学式等.


 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:解答题
| 测定 序号 | 待测液体积/mL | 标准液滴定管起点读数/mL | 标准液滴定管终点读数/mL |
| 1 | 25.00 | 0.06 | 24.04 |
| 2 | 25.00 | 0.02 | 24.02 |
| 3 | 25.00 | 0.12 | 24.14 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实际应称Na2CO3质量/g | 应选用容量瓶的规格/mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba2+、Cl-、NO3-、K+ | B. | HCO3-、K+、SO42-、Cl- | ||
| C. | Fe2+、Cl-、Na+、NO3- | D. | Na+、Cl-、K+、SO42-、 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaCl2溶液和K2SO4溶液反应 | B. | Al放入烧碱溶液中 | ||
| C. | NaOH溶液和CuSO4溶液反应 | D. | KSCN溶液和FeCl3溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
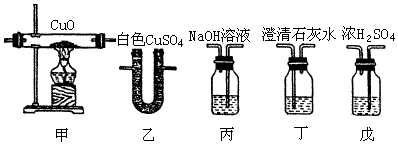
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液.
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液.| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点(℃) | 34.7 | 78.5 | 118 | 77.1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com