
新型净水剂高铁酸钾(K2FeO4)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定。工业上制备K2FeO4的常用方法有两种。
方法Ⅰ:次氯酸盐氧化法。工艺流程如下图所示。
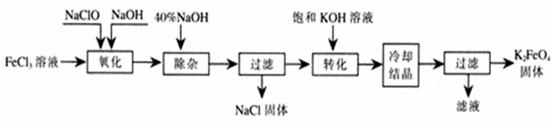
⑴ 写出“氧化”过程中反应的化学方程式: 。
⑵写出“转化”过程中发生反应的化学方程式为 。
⑶上述工艺得到的高铁酸钾常含有杂质,可用重结晶发提纯,操作是:将粗产品用 溶解,然后 。
方法Ⅱ:电解法。以铁为阳极电解氢氧化钠溶液,然后在阳极溶液中加入KOH。
⑷电解时阳极发生反应生成FeO42-,该电极反应方程式为 。
科目:高中化学 来源: 题型:
Na2CO3固体中可能含有杂质K2CO3、NaHCO3、NaCl中一种或几种,取10.6g样品,加入足量的稀盐酸产生气体4.8g,下列分析正确的是()
| A. | 一定含有NaHCO3 | B. | 一定含有K2CO3 | |
| C. | 一定不含NaCl | D. | 一定含有NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
“绿色化学”对化学反应提出了“原子经济性”(原子节约)的新概念及要求,理想原子经济性反应是原料分子中的原子全部转化成所需要的产物,不产生副产物,实现零排放。下列反应类型一定符合这一要求的是( )
①取代反应 ②加成反应 ③消去反应 ④水解反应 ⑤加聚反应 ⑥缩聚反应 ⑦酯化反应
A.①④ B.②③
C.⑤⑥ D.②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在指定溶液中,能大量共存的是 ( )
①无色溶液中:K+,Cl-,Ca2+,CO33-,SO42-,NO3-
②pH=11的溶液中:CO32-,Na+,[Al(OH)4]-,NO3-,S2-,SO32-
③水电离的H+浓度c(H+)=10-12mol·L-1的溶液中:Cl-,CO32-,NO3-,NH4+,SO32-
④加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,K+,SO42-
⑤使石蕊变红的溶液中:Fe2+,MnO4-,NO3-,Na+,SO42-
⑥中性溶液中:Fe3+,Al3+,NO3-,I-,Cl-,S2-
A.①②⑤ B.①③⑥ C.②④ D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
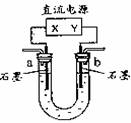
用右图装置(X、Y是直流电源的两极)分别进行下列各组实验,则下表中所列各项对应关系均正确的一组是 ( )
| 选项 | 电源X极 | 实验前U形管中液体 | 通电后现象及结论 |
| A | 正极 | Na2SO4溶液 | U形管两端滴入酚酞后, a管中呈红色 |
| B | 正极 | AgNO3溶液 | b管中电极反应式是4OH—4e-=2H2O+O2↑ |
| C | 负极 | KCl和CuCl2混合溶液 | 相同条件下,a、b两管中产生的气体总体积可能相等 |
| D | 负极 | AlCl3溶液 | a管中先产生白色沉淀后沉淀溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
m mol乙炔跟n mol氢气在密闭容器中反应,当其达到平衡时,生成p mol乙烯,将平衡混合气体完全燃烧生成CO2和H2O,所需氧气的物质的量是( )
A.(3m+n)mol B.(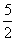 m+
m+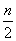 -3p)mol C.(3m+n+2p)mol D.(
-3p)mol C.(3m+n+2p)mol D.( 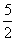 m+
m+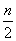 )mol
)mol
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机化合物的结构如图
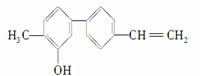
关于该化合物的下列说法正确的是( )
A.由于含有氧元素不是有机物
B.完全燃烧时只有二氧化碳和水两种产物
C.分子中含有羟基属于醇
D.不能使溴水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示。已知YW的原子充数之和是Z的3倍,下列说法正确的是( )
| Y | Z | ||
| X | W |
A.原子半径:X<Y<Z
B.气态氢化物的稳定性:X>Z
C.Z、W均可与Mg形成离子化合物
D.最高价氧化物对应水化物的酸性:Y>W
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com