
4A(s)+3B(g)═2C(g)+D(g),经2min后B的浓度减少0.6mol•L﹣1.对此反应速率的表示正确的是()
A. 用A表示的反应速率是0.4mol•L﹣1•min﹣1
B. 分别用B、C、D表示反应速率,其比值是3:2:1
C. 在2min末的反应速率,用B表示是0.3mol•L﹣1•min﹣1
D. 在2min内的反应速率,用C表示是0.3mol•L﹣1•min﹣1
考点: 化学反应速率和化学计量数的关系.
专题: 化学反应速率专题.
分析: A.化学反应速率表示单位时间内浓度的变化量,固体或纯液体的浓度一般视为常数,一般也不用固体或纯液体来表示反应速;
B.不同物质表示的速率之比等于其化学计量数之比;
C.化学反应速率为一段时间内平均速率,不是即时速率;
D.浓度变化量之比等于其化学计量数之比,据此计算△c(C),再根据v=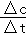 计算v(C).
计算v(C).
解答: 解:A.物质A是固体,浓度不变,不能用A表示该反应的反应速率,故A错误;
B.不同物质表示的速率之比等于其化学计量数之比,则v(B):v(C):v(D)=3:2:1,故B正确;
C.2min末的反应速率为即时速率,用B表示速率0.3mol/(L∙min),是2min内的平均速率,故C错误;
D.2min内△c(C)=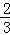 △c(B)=0.4mol/L,故2min内的v(C)=
△c(B)=0.4mol/L,故2min内的v(C)=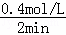 =0.2mol•L﹣1•min﹣1,故D错误.
=0.2mol•L﹣1•min﹣1,故D错误.
故选B.
点评: 本题考查对化学反应速率的理解及有关计算,难度不大,注意固体或纯液体的浓度一般视为常数,故增加或减少固体或纯液体的量,化学反应速率不变,一般也不用固体或纯液体来表示反应速,化学反应速率为一段时间内平均速率,不是即时速率.


科目:高中化学 来源: 题型:
下列实验现象预测正确的是()
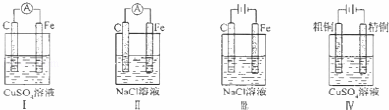
A. 实验Ⅰ:电流表A指针偏转,碳棒上有气泡冒出
B. 实验Ⅱ:电流表A指针偏转,铁极上有无色气体产生
C. 实验Ⅲ:碳棒上有无色气体产生,铁极上有黄绿色气体产生
D. 实验IV:粗铜溶解,精铜上有红色固体析出
查看答案和解析>>
科目:高中化学 来源: 题型:
向10mL 0.1mol•L﹣1 NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液x mL,下列叙述正确的是()
A. x=10时,溶液中有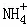 、Al3+、
、Al3+、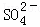 ,且c(
,且c(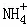 )=c(Al3+)
)=c(Al3+)
B. x=20时,溶液中所发生的反应离子方程式为:Al3++2SO42﹣+2Ba2++4OH﹣═2BaSO4↓+AlO2﹣+2H2O
C. x=30时,溶液中有Ba2+、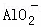 、OH﹣,且c(OH﹣)>c(
、OH﹣,且c(OH﹣)>c(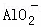 )
)
D. 滴加过程中,生成沉淀的最大物质的量为0.003mol
查看答案和解析>>
科目:高中化学 来源: 题型:
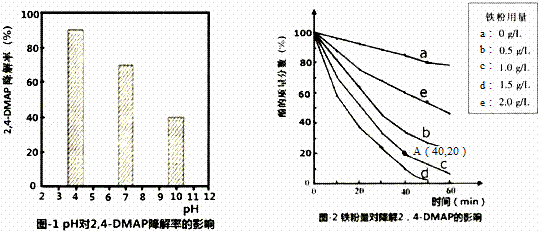
利用Na2S2O8产生的强氧化性SO4﹣•(自由基)降解有机污染物是目前最具潜力的高级氧化技术.文献报道某课题组探究pH,单质铁和Na2S2O8的浓度对降解2,4﹣DMAP(2,4﹣﹣甲基苯酚)效率的影响.
(1)探究溶液酸碱性的影响:将等量的2,4﹣DMAP加入到不同pH的Na2S2O8溶液中,结果如图1所示.由此可知:溶液酸性增强, (填“有利于”或“不利于”)Na2S2O8产生SO4﹣•.
(2)探究铁粉用量的影响:
①实验前,先用0.1mol•L﹣1 H2SO4洗涤Fe粉,其目的是 ,后用蒸馏水洗涤至中性;
②相同条件下,取不同量处理后的铁粉分别加入c(2,4﹣DMAP)=1.0×10 ﹣3mol•L﹣1、c(Na2S2O8)=4.2×10﹣3mol•L﹣1的混合溶液中,实验结果如图2所示.其中降解效率最好的铁粉用量是1.5g/L;计算从反应开始到A点时,2,4﹣DMAP降解的平均反应速率为 (忽略反应过程中溶液总质量变化).
③已知:2Fe+O2+2H2O=2Fe2++4OH﹣,S2O8﹣+Fe2+=SO4﹣+SO42﹣+Fe3+此外还可能会发生:SO4﹣+Fe2+=SO42﹣+Fe3+.当铁粉加入量过大时,2,4﹣DMAP的降解率反而下降,原因可能是(用离子方程式表示). .
(3)探究Na2S2O8浓度的影响:填写下表中空格,完成实验方案.
序号、物理量 M(Fe粉)/g V/mL V/mL 收集数据和得出结论
1 100 0.3 50 50
2 100V(污水)/mL 0.3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学反应速率的说法正确的是()
A. 化学反应速率是指一定时间内任何一种反应物浓度的减少或者任何一种生成物浓度的增加
B. 化学反应速率为“0.8mol/(L•s)”表示的意思是:时间为1s时,某物质的浓度为0.8mol/L
C. 根据化学反应速率的大小可以知道化学反应进行的快慢
D. 对于任何化学反应来说,反应速率越大,反应现象越明显
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实能说明影响化学反应速率的决定性因素是反应物本身性质的是()
A. Cu能与浓硝酸反应,而不与浓盐酸反应
B. Cu与浓硝酸反应比与稀硝酸反应快
C. N2与O2在常温、常压下不反应,放电时可反应
D. Fe与浓盐酸反应快,与稀盐酸反应慢
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是()
A. 反应物分子(或离子)间的每次碰撞是反应的先决条件
B. 反应物的分子的每次碰撞都能发生化学反应
C. 活化分子具有比普通分子更高的能量,催化剂能够减低活化能的数值
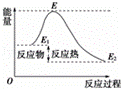
D. 活化能是活化分子的平均能量与所有分子平均能量之差,如图所示正反应的活化能为E﹣E1
查看答案和解析>>
科目:高中化学 来源: 题型:
如图装置中发生反应的离子方程式为:Zn+2H+═Zn2++H2↑,下列说法错误的是()

A. a、b不可能是同种材料的电极
B. 该装置可能是电解池,电解质溶液为稀盐酸
C. 该装置可能是原电池,电解质溶液为稀盐酸
D. 该装置可看作是铜﹣锌原电池,电解质溶液是稀硫酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com