
【题目】酸、碱、盐均属于电解质,它们的水溶液中存在各种平衡.
(1)氨水是中学常见碱
①下列事实可证明氨水是弱碱的是(填字母序号).
A.氨水能跟氯化亚铁溶液反应生成氢氧化亚铁
B.常温下,0.1molL﹣1氨水pH为11
C.铵盐受热易分解
D.常温下,0.1molL﹣1氯化铵溶液的pH为5
②下列方法中,可以使氨水电离程度增大的是(填字母序号).
A.通入氨气 B.加入少量氯化铁固体 C.加水稀释 D.加入少量氯化铵固体
(2)盐酸和醋酸是中学常见酸
用0.1molL﹣1NaOH溶液分别滴定体积均为20.00mL、浓度均为0.1molL﹣1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线.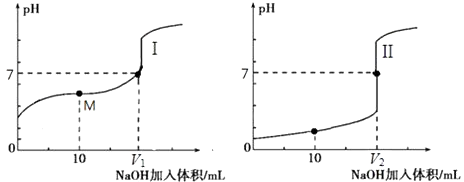
①滴定醋酸的曲线是(填“I”或“II”).
②滴定开始前,三种溶液中由水电离出的c(H+)最大的是 .
③V1和V2的关系:V1V2(填“>”、“=”或“<”).
④M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是 .
【答案】
(1)BD;BC
(2)I;0.1mol?L﹣1醋酸溶液;<;c(CH3COO﹣)>c (Na+)>c (H+)>c (OH﹣)
【解析】解:(1)①A.氨水和氯化亚铁反应生成氢氧化亚铁沉淀,说明一水合氨是碱,但不能说明一水合氨部分电离,所以不能说明是弱电解质,故A错误;
B.常温下,0.1molL﹣1氨水pH为11,溶液呈酸性,说明一水合氨部分电离,则说明一水合氨是弱电解质,故B正确;
C.铵盐受热易分解说明铵盐不稳定,不能说明一水合氨部分电离,则不能说明一水合氨是弱电解质,故C错误;
D.常温下,0.1mol/L的氯化铵溶液pH约为5,溶液呈酸性,说明氯化铵是强酸弱碱盐,则说明一水合氨是弱电解质,故D正确;
所以答案是:BD;
②A.通入氨气,氨水的浓度增大,电离程度减小,故A错误;
B.加入少量氯化铁固体,会消耗氢氧根离子,则促进一水合氨的电离,电离程度增大,故B正确;
C.加水稀释,促进一水合氨的电离,电离程度增大,故C正确;
D.加入少量氯化铵固体,铵根离子浓度增大,抑制氨水的电离,电离程度减小,故D错误;
所以答案是:BC;(2)①由图中未加NaOH时的pH可知,图Ⅰ中酸的pH大于1,图Ⅱ中酸的pH=1,说明Ⅱ为0.1mol/L的盐酸溶液,为醋酸溶液滴定过程,所以滴定醋酸的曲线是I,
所以答案是:I;
②0.1molL﹣1 NaOH溶液、0.1molL﹣1的盐酸中氢离子和氢氧根浓度都是0.1mol/L,对水的抑制作用一样,但是0.1mol/L醋酸溶液中氢离子浓度小于0.1mol/L,所以对水的电离抑制较小,即三种溶液中由水电离出的c(H+)最大的是0.1 molL﹣1醋酸溶液,所以答案是:0.1molL﹣1醋酸溶液;
③醋酸和氢氧化钠之间的反应,当恰好完全反应得到的醋酸钠显示碱性,要使得溶液显示中性,pH=7,需要醋酸稍过量,所以盐酸和氢氧化钠恰好完全反应,得到的氯化钠显示中性,所以V1<V2 , 所以答案是:<;
④用0.1molL﹣1 NaOH溶液10mL和溶液体积为20.00mL0.1molL﹣1的醋酸反应,得到的是醋酸和醋酸钠的混合物,显示酸性,此时离子浓度大小c(CH3COO﹣)>c (Na+)>c (H+)>c (OH﹣),所以答案是:c(CH3COO﹣)>c (Na+)>c (H+)>c (OH﹣).
【考点精析】认真审题,首先需要了解弱电解质在水溶液中的电离平衡(当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理).


科目:高中化学 来源: 题型:
【题目】反应①Fe(s)+CO2(g)FeO(s)+CO(g)△H1=akJmol﹣1 , 平衡常数为K;反应②CO(g)+ ![]() O2(g)CO2(g)△H2=bkJmol﹣1 . 测得在不同温度下,K值如表:
O2(g)CO2(g)△H2=bkJmol﹣1 . 测得在不同温度下,K值如表:
温度/℃ | 500 | 700 | 900 |
K | 1.00 | 1.47 | 2.40 |
(1)若500℃时进行反应①,CO2起始浓度为2mol/L,CO的平衡浓度为 .
(2)反应①中的a0(填“大于”、“小于”或“等于”).
(3)700℃时反应①达到平衡,要使得该平衡向右移动,其他条件不变时,可以采取的措施有(填序号).
A.缩小反应器体积
B.通入CO2
C.升高温度到 900℃
D.使用合适的催化剂
(4)如图图象符合反应①的是(填序号)(图中φ是混合物中CO的含量;T为温度).
(5)反应③2Fe(s)+O2(g)═2FeO(s)△H3= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子.元素Y的负一价离子的最外层电子数与次外层的相同.回答下列问题:
(1)单质M的晶体类型为 , 晶体中原子间通过作用形成面心立方密堆积,其中M原子的配位数为 .
(2)元素Y基态原子的核外电子排布式为 , 其同周期元素中,第一电离能最大的是(写元素符号).元素Y的含氧酸中,酸性最强的是(写化学式),该酸根离子的立体构型为 .
(3)M与Y形成的一种化合物的立方晶胞如图所示. ①该化合物的化学式为 , 已知晶胞参数a=0.542nm,此晶体的密度为gcm﹣3 . (写出计算式,不要求计算结果.阿伏加德罗常数为NA)
②该化合物难溶于水但易溶于氨水,其原因是 . 此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置正确且能达到实验目的是( )
A.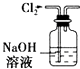 用如图所示装置除去Cl2中含有的少量HCl
用如图所示装置除去Cl2中含有的少量HCl
B.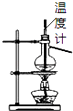 如图所示为石油分馏
如图所示为石油分馏
C.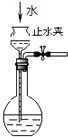 如图所示为检查装置气密性
如图所示为检查装置气密性
D.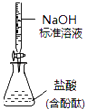 如图所示为测定未知盐酸的浓度
如图所示为测定未知盐酸的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同温度下,向2L密闭容器中加入1molNO和1mol活性炭,发生反应:2NO(g)+C(s)═N2(g)+CO2(g)△H=﹣213.5kJ mol﹣1 , 达到平衡时的数据如下:
温度/℃ | n(活性炭)/mol | n(CO2)/mol |
T1 | 0.70 | |
T2 | 0.25 |
下列说法不正确的是( )
A.上述信息可推知:T1<T2
B.T1℃时,该反应的平衡常数K= ![]()
C.T1℃时,若开始时反应物的用量均减小一半,平衡后NO的转化率减小
D.T2℃时,若反应达平衡后再缩小容器的体积,c(N2):c(NO)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知金属活动相差越大,形成原电池时越容易放电.请根据如图装置,回答下列问题: 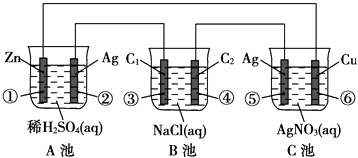
(1)各装置名称是:A池 , B池 .
(2)写出电极上发生的反应:① , ③ , ⑤ .
(3)当电路上有2mol电子流过时,①极上质量变化g,⑥极上质量变化g.
(4)反应进行一段时间后,A,B,C三池中电解质溶液浓度不变的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前市场上有一种专门为婴幼儿设计的电解质饮料,适合在婴幼儿感冒、发烧时快速补充体内流失的电解质成分。下列物质可用作该饮料中的电解质的是
A.Fe B.葡萄糖 C.MgSO4 D.CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子,在所给的条件下,一定能够大量共存的是( )
A.在滴加酸碱指示剂酚酞试液后呈现红色的溶液中:Na+、Cl﹣、AlO2﹣、CO32﹣
B.在由水电离出的c(H+)=1×10﹣12mol/L的溶液中:HCO3﹣、Al3+、NH4+、ClO﹣
C.在 ![]() =1×1012的溶液中:Fe2+、Mg2+、CO32﹣、NO3﹣
=1×1012的溶液中:Fe2+、Mg2+、CO32﹣、NO3﹣
D.在AlCl3溶液中:K+、NO3﹣、S2﹣、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含有H2SO4的H2O2溶液中滴加一定量的KMnO4溶液,反应开始后,溶液中Mn2+的浓度c将随时间t的变化而变化。某学生在做实验前认为,Mn2+的浓度c与时间t的关系如图甲所示,做完实验后,得到的结果如图乙所示。请回答下列问题:

(1)写出H2O2与KMnO4反应的化学方程式 。
(2)Oa段的意义为 。
(3)ab段的意义及ab段陡的原因为 。
(4)bc段的意义为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com