
【题目】
新型储氢材料是氢能的重要研究方向。
(1)化合物A(H3BNH3)是一种潜在的储氢材料,可由六元环状物质(HB=NH)3通过如下反应制得:3CH4+2(HB=NH)3+6H2O=3CO2+6H3BNH3。A在一定条件下通过多步去氢可最终转化为氮化硼(BN)。
①基态O原子的电子占据了___________个能层,最高能级有___________种运动状态不同的电子。
②CH4、H2O、CO2分子键角从大到小的顺序是___________。生成物H3BNH3中是否存在配位键___________(填“是”或“否”)。
(2)掺杂T基催化剂的NaAlH4是其中一种具有较好吸、放氢性能的可逆储氢材料。NaAlH4由Na+和AlH4-构成,与AlH4-互为等电子体的分子有____(任写一个),Al原子的杂化轨道类型是____。Na、Al、H元素的电负性由大到小的顺序为_____。
(3)Ni和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在中国已实现了产业化。该合金的晶胞结构如图所示。
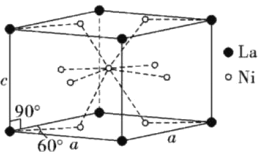
①该晶体的化学式为___________。
②已知该晶胞的摩尔质量为Mg/mol,密度为dg/cm3。设NA为阿伏加徳罗常数的值,则该晶胞的体积是___________cm3(用含M、d、NA的代数式表示)。
③已知晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子比较温定,晶胞参数分别为apm、apm、cpm。标准状况下氢气的密度为Mg/cm3;若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为___________。(用相关字母表示已知储氢能力=![]() )。
)。
【答案】2 4 CO2>CH4>H20 是 CH4 sp3 H>Al>Na LaNi5 M/NA![]() d 6
d 6![]() 1030/(NA
1030/(NA![]() a2
a2![]() c
c![]() sin60
sin60![]() M)
M)
【解析】
(1)①基态O原子的核外电子排布为1s22s22p4,分别占据K、L能层,1s、2s、2p三个能级,2p为最高能级排布4个电子,有4种不同的运动状态;答案:2;4。
②CH4是正四面体结构,键角109![]() 28,;H2O是V型分子,键角104
28,;H2O是V型分子,键角104![]() 30,;CO2是直线型分子,键角为180
30,;CO2是直线型分子,键角为180![]() , CH4、H2O、CO2分子键角从大到小的顺序是CO2>CH4>H2O;在H3BNH3中的B与N原子之间存在配位键。答案:CO2>CH4>H2O;是。
, CH4、H2O、CO2分子键角从大到小的顺序是CO2>CH4>H2O;在H3BNH3中的B与N原子之间存在配位键。答案:CO2>CH4>H2O;是。
(2) AlH4-为含有5个原子的阴离子,价电子数为3+1![]() 4+1=8,与AlH4-互为等电子体的分子有CH4。AlH4-的中心原子价层电子对数为4,且中心原子不含孤对电子,所以其立体构型是正四而体形,Al原子的杂化轨道类型是sp3杂化。金属性越强,电负性越小,其电负性由大到小的顺序为H>Al>Na。答案:CH4;sp3;H>Al>Na。
4+1=8,与AlH4-互为等电子体的分子有CH4。AlH4-的中心原子价层电子对数为4,且中心原子不含孤对电子,所以其立体构型是正四而体形,Al原子的杂化轨道类型是sp3杂化。金属性越强,电负性越小,其电负性由大到小的顺序为H>Al>Na。答案:CH4;sp3;H>Al>Na。
(3) 根据该合金的晶胞图可知,晶胞中心有一个镍原子,其他8个镍原子都在晶胞面上,镧原子都在晶胞顶点,所以晶胞实际含有的镍原子为1+1/2![]() 8=5,晶胞实际含有的镧原了为8
8=5,晶胞实际含有的镧原了为8![]() 1/8=1,所以晶体的化学式LaNi5。答案:LaNi5。
1/8=1,所以晶体的化学式LaNi5。答案:LaNi5。
②一个晶胞的质量m=M/NA,根据m=![]() V=V
V=V![]() d即V=M/NA
d即V=M/NA![]() d;答案:M/NA
d;答案:M/NA![]() d。
d。
③LaNi5合金储氢后的密度p=m(晶胞中的H)/V(晶胞)=1![]() 6/ [NA
6/ [NA![]() (a
(a![]() 10-10)2
10-10)2![]() c
c![]() 10-10
10-10![]() sin60
sin60![]() ],由定义式可知储氢能力=
],由定义式可知储氢能力=![]()
=6![]() 1030/(NA
1030/(NA![]() a2
a2![]() c
c![]() sin60
sin60![]() M)
M)


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是![]()
![]()
A. 标准状况下,22.4LCO和CO2的混合物中,含碳原子的数目为NA
B. 14g分子式为C5H10的烃中,含有的碳碳双键的数目为0.2NA
C. 0.1mol/L的CH3COONH4溶液中,含铵根离子数目小于0.1NA
D. 标准状况下2.24LCl2通入足量水中或NaOH溶液中,转移电子数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
I、甲同学向1molL﹣1氯化铁溶液中加入少量的NaOH溶液;
II、乙同学直接加热饱和FeCl3溶液;
III、丙同学向25ml沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热。试回答下列问题:
(1)其中操作正确的同学是___。写出此过程中的化学方程式:___;
(2)证明有Fe(OH)3胶体生成的最简单实验操作是___;
(3)丁同学利用所制得的Fe(OH)3胶体进行下列实验:
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶粒带__电荷。
②向其中加入饱和Na2SO4溶液,产生的现象是____;
③向所得Fe(OH)3胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为___;继续滴加,沉淀最终消失且得棕黄色溶液,写出化学方程式___;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋是一个巨大的宝藏,期待着人们的开发和利用。
Ⅰ.(1)利用海水可以得到食盐,从海水中得到食盐的变化是___变化。(填“物理”或“化学”)
(2)要除去某食盐晶体中的CaCl2、MgCl2、Na2SO4等杂质,有以下操作:
A.蒸发结晶 B.过滤 C.加入过量的Na2CO3溶液 D.加水溶解 E.加入过量的烧碱溶液 F.加入过量稀盐酸 G.加入过量的Ba(NO3)2溶液 H.加入过量的稀硝酸 I.加入过量的BaCl2溶液
正确的操作顺序是:__→E→___→C→__→__→A
Ⅱ.海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如图所示:
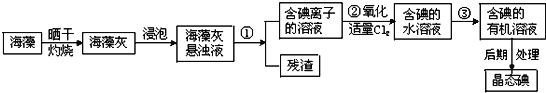
(1)指出提取碘的过程中有关的实验操作名称:①___③___。
(2)操作③中可以选择的有机试剂为___,选择该试剂时,水层在___层(填 “上”或“下”),含碘溶液应从___(获得填“容器上口”或“容器下口”),要从碘的有机溶液中获得碘单质,应采用___的操作(填一种实验操作方法)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A2+B2![]() 2AB在不同条件下,产物AB百分含量随时间变化关系如图所示,a为500℃,b为300℃时情况,c为300℃时从时间t3开始向容器中加压的情况,则下列叙述正确的是
2AB在不同条件下,产物AB百分含量随时间变化关系如图所示,a为500℃,b为300℃时情况,c为300℃时从时间t3开始向容器中加压的情况,则下列叙述正确的是
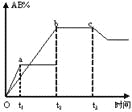
A. A2、B2、AB均为气体,正反应放热
B. AB为气体,A2、B2中最少有一种为非气体,正反应放热
C. AB为气体,A2、B2中最少有一种为非气体,正反应吸热
D. AB为固体,A2、B2中最少有一种为非气体,正反应吸热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某硫原子的质量是ag,12C原子的质量是bg,若NA只表示阿伏加德罗常数的数值,则下列说法中正确的是( )
①该硫原子的相对原子质量为![]() ②mg该硫原子的物质的量为
②mg该硫原子的物质的量为![]() mol
mol
③该硫原子的摩尔质量是aNA g ④ag该硫原子所含的电子数为16NA
A. ①③ B. ②④ C. ①② D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废水中含有的![]() 和CrO42-会对水体产生很大的危害,这种工业废水必须净化处理。一种处理含铬废水的工艺流程如下:
和CrO42-会对水体产生很大的危害,这种工业废水必须净化处理。一种处理含铬废水的工艺流程如下:
![]()
下列说法不正确的是
A. ①中,酸化后发生反应为![]()
B. ②中,反应的氧化剂与还原剂的物质的量之比为3∶1
C. ③中,所得沉淀Cr(OH)3中含有Fe(OH)3
D. ③中调pH所用物质可以是NH3或Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10mol·L-1NaOH溶液分别滴定20.00mL浓度均为0.10mol·L-1CH3COOH溶液和HCN溶液所得滴定曲线如下图。下列说法正确的是
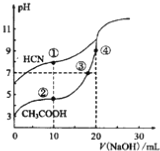
A. 点①和点②所示溶液中:c(CH3COO-)<c(CN-)
B. 点①和点②所示溶液中:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH)
C. 点④所示溶液液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D. 点②和点③所示溶液中都有:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积恒为0.5 L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,其化学平衡常数K与t的关系如下表:
2NH3(g) ΔH<0,其化学平衡常数K与t的关系如下表:
t/℃ | 200 | 300 | 400 |
K | K1 | K2 | 0.5(mol·L-1)-2 |
请完成下列问题:
(1)试比较K1、K2的大小,K1________K2(填“>”、“=”或“<”)。
(2)下列各项能做为判断该反应达到化学平衡状态的依据的是_____(填字母序号)。
a.容器内N2、H2、NH3的浓度之比为1∶3∶2
b.v正(N2)=3v逆(H2)
c.容器内压强保持不变
d.混合气体的密度保持不变
(3)400 ℃时,反应2NH3(g)![]() N2(g)+3H2(g)的平衡常数K为____。当测得NH3、H2、N2的物质的量分别为3 mol、1 mol、2 mol时,则该反应的v正(N2)___ v逆(N2)(填“>”、“=”或“<”)。
N2(g)+3H2(g)的平衡常数K为____。当测得NH3、H2、N2的物质的量分别为3 mol、1 mol、2 mol时,则该反应的v正(N2)___ v逆(N2)(填“>”、“=”或“<”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com