
| A、稀的食盐水能杀死H7N9禽流感病毒 |
| B、涤纶、塑料、光导纤维都是有机高分子材料 |
| C、用电镀厂的废水直接灌溉农田,可提高水的利用率 |
| D、外形似海绵、密度小、有磁性的碳与石墨互为同素异形体 |


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:
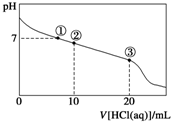 常温下,向20.00mL 0.100mol?L-1 CH3COONa溶液中逐滴加入0.1000mol?L-1盐酸,溶液的pH与所加盐酸体积的关系如图所示(不考虑挥发).下列说法正确的是( )
常温下,向20.00mL 0.100mol?L-1 CH3COONa溶液中逐滴加入0.1000mol?L-1盐酸,溶液的pH与所加盐酸体积的关系如图所示(不考虑挥发).下列说法正确的是( )| A、点①所示溶液中:c(CH3COOH)=c(Cl-)>c(Na+)>c(OH-)=c(H+) |
| B、点②所示溶液中:c(Na+)>c(CH3COO-)>c(Cl-)>c(CH3COOH) |
| C、点③所示溶液中:c(CH3COOH)>c(Na+)>c(H+)>c(CH3COO-) |
| D、整个过程中可能出现:c(H+)+c(Na+)=c(CH3COOH)+c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,8g O2含有4NA个电子 |
| B、1L 0.1mol?L-1的氨水中有NA个NH4+ |
| C、常温常压下,22.4L氯气与足量的镁粉反应,转移的电子数为2NA |
| D、1mol Na在空气中燃烧失去2NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某些金属化合物具有特定的颜色,因此可制作烟花 |
| B、石油的催化裂化及裂解可以得到较多的轻质油和气态烯烃 |
| C、Mg、Fe等金属在一定条件下与水反应都生成H2和对应的氢氧化物 |
| D、蛋白质溶液中加入浓的硫酸钠溶液,有沉淀析出,这种作用称为变性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:Z<Y<W,而离子半径:W<Y<Z |
| B、W的氯化物水瑢液中滴加过量Z与钠形成的饱和溶液,可生成W配合物 |
| C、若由X、Y、Z组成盐的水溶液呈酸性,则溶液中该盐阳离子浓度大于酸根离子浓度 |
| D、已知YX3沸点远高于YZ3,则Y-X键的键能高于Y-Z键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10mL 0.2 mol?L-1的氨水与10mL 0.1mol?L-1的盐酸充分反应混合后的溶液中,存在:c(NH4+)+c(NH3?H2O)=2c(Cl-)=0.1mol?L-1 |
| B、已知酸性HF>CH3COOH,物质的量浓度相等的NaF与CH3COOK溶液中:c(Na+)-c(F-)>c(K+)-c(CH3COO-) |
| C、CH3COOK溶液中加入少量NaNO3固体后的碱性溶液一定有:c(K+)+c(H+)=c(CH3COO-)+c(OH-) |
| D、NaHSO3溶液中一定有:c(Na+)>c(HSO3-)>c(SO32-)>c(H2SO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、放热反应不需加热即可发生 |
| B、化学反应均伴随有能量变化,这种能量变化除热能外,还可以是光能、电能等 |
| C、可燃物的燃烧热的大小与参与反应的可燃物的多少无关 |
| D、化学反应热效应数值与参与反应的物质多少有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、气态氢化物的稳定性:X>W |
| B、单质的还原性:Y>Z |
| C、原子半径:Y<Z<W |
| D、Y和Z两者最高价氧化物对应的水化物能相互反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| CaSO4 | Mg2(OH)2CO3 | CaCO3 | BaSO4 | BaCO3 |
| 2.6×10-2 | 2.5×10-4 | 7.8×10-4 | 2.4×10-4 | 1.7×10-3 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com