
【题目】稀释0.1mol·L-1的CH3COOH溶液过程中,以下各项数值增大的是()
A.n(H+)B.c(CH3COO-)
C.![]() D.
D.![]()
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
【题目】下图为一定条件下采用多孔惰性电极的储氢电池充电装置(忽略其他有机物)。已知储氢装置的电流效率![]() ×100%,下列说法不正确的是
×100%,下列说法不正确的是
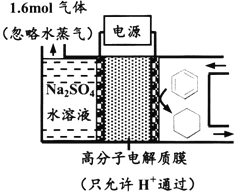
A. 采用多孔电极增大了接触面积,可降低电池能量损失
B. 过程中通过C-H键的断裂实现氢的储存
C. 生成目标产物的电极反应式为C6H6+6e-+6H+===C6H12
D. 若![]() =75%,则参加反应的苯为0.8mol
=75%,则参加反应的苯为0.8mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐中含有一定量的镁、铁等杂质,加碘盐可能含有 K+、IO3-、I-、Mg2+.加碘盐中碘的损失主要是由于杂质、水分、空气中的氧气以及光照、受热引起的。
已知:IO3-+5I-+6H+→3I2+3H2O,2Fe3++2I-→2Fe2++I2,KI+I2KI3;氧化性: IO3->Fe3+>I2。
(1)学生甲对某加碘盐进行如下实验,以确定该加碘盐中碘元素的存在形式。取一定量加碘盐,用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为 3 份。第一份试液中滴加 KSCN 溶液后显红色;第二份试液中加足量 KI 固体,溶液显淡黄色,加入 CCl4,下层溶液显紫红色;第三份试液中加入适量 KIO3 固体后,滴加淀粉试剂,溶液不变色。
①第一份试液中,加 KSCN 溶液显红色,该红色物质是______(用化学式表示)。
②第二份试液中“加入 CCl4”的实验操作名称为______,CCl4 中显紫红色的物质是______(用化学式表示)。
③根据这三次实验,学生甲得出以下结论:
在加碘盐中,除了 Na+、Cl-以外,一定存在的离子是______,可能存在的离子是______,一定不存在的离子是______。由此可确定,该加碘盐中碘元素是______价(填化合价)的碘。
(2)将 I2溶于 KI 溶液,在低温条件下,可制得 KI3H2O.该物质作为食盐加碘剂是否合适?______(填“是”或“否”),并说明理由______。
(3)已知:I2+2S2O32-→2I-+S4O62-.学生乙用上述反应方程式测定食用精制盐的碘含量(假设不含Fe3+),其步骤为:
a.准确称取 wg 食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量 KI 溶液,使 KIO3与 KI 反应完全;
c.以淀粉溶液为指示剂,逐滴加入物质的量浓度为 2.0×10-3mol/L 的 Na2S2O3 溶液 10.0mL,恰好反应完全。
根据以上实验,学生乙所测精制盐的碘含量(以 I 元素计)是______mg/kg(以含w的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用含三价钒(V2O3)为主的某石煤为原料(含有 Al2O3、CaO 等杂质),钙化法焙烧制备 V2O5,其流程如下:
![]()
(资料)+5 价钒在溶液中的主要存在形式与溶液 pH 的关系:
pH | 4~6 | 6~8 | 8~10 | 10~12 |
主要离子 | VO2+ | VO3- | V2O74- | VO43- |
(1)焙烧: 向石煤中加生石灰焙烧,将 V2O3 转化为 Ca(VO3)2 的化学方程式是______________。
(2)酸浸:①Ca(VO3)2 难溶于水,可溶于盐酸。若焙砂酸浸时溶液的 pH=4,Ca(VO3)2 溶于盐酸的离子方程式是________。
②酸度对钒和铝的溶解量的影响如图所示:酸浸时溶液的酸度控制在大约 3.2%,根据下图推测,酸浸时不选择更高酸度的原因是________________。
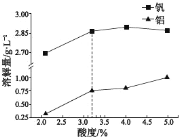
(3)转沉: 将浸出液中的钒转化为 NH4VO3 固体,其流程如下:
![]()
①浸出液中加入石灰乳的作用是_____。
②向(NH4)3VO4 溶液中加入 NH4Cl 溶液,控制溶液的 pH=7.5。当 pH>8 时,NH4VO3 的产量明显降低,原因是_______________。
(4)测定产品中 V2O5 的纯度:称取 ag 产品,先用硫酸溶解,得到(VO2)2SO4 溶液。再加入 b1mLc1mol/L(NH4)2Fe(SO4)2 溶液(VO2++2H++Fe2+=VO2++Fe3++H2O) 最后用 c2mol/LKMnO4 溶液滴定过量的(NH4)2Fe(SO4)2 至终点,消耗 KMnO4 溶液的体积为 b2mL。已知 MnO4-被还原为 Mn2+,假设杂质不参与反应。则产品中 V2O5 的质量分数是_____。(V2O5 的摩尔质量::182g/mol)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用0.100 mol·L-1盐酸分别滴定20.00 mL 0.100 mol·L-1的氨水和20.00 mL 0.100 mol·L-1NaOH溶液,两溶液的pH与所加盐酸体积(V)的关系如图所示。下列说法正确的是 ( )
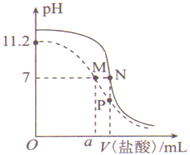
A. Kb(NH3·H2O)的数量级为10—4
B. 10 < a < 20
C. P点溶液中:c(NH4+)>c(Cl一)
D. 水的电离程度:M > N > P
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A+B→C △H <0,分两步进行 ① A+B→X △H>0 ② X→C △H<0 。下列示意图中,能正确表示总反应过程中能量变化的是
A. 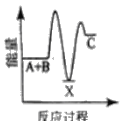 B.
B. 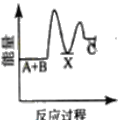
C. 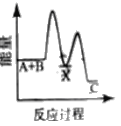 D.
D. 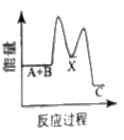
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是( )
①Al2O3 ![]() NaAlO2(aq)
NaAlO2(aq)![]() Al(OH)3
Al(OH)3
②S ![]() SO3
SO3 ![]() H2SO4
H2SO4
③饱和NaCl(aq)![]() NaHCO3
NaHCO3 ![]() Na2CO3
Na2CO3
④Fe2O3 ![]() FeCl3(aq)
FeCl3(aq)![]() 无水FeCl3
无水FeCl3
⑤MgCl2(aq)![]() Mg(OH)2
Mg(OH)2![]() MgO
MgO
A. ②③④ B. ①③⑤ C. ②④⑤ D. ①④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】容积固定为3L的某密闭容器中加入1mol A、2mol B,一定温度下发生如下发应:A(s)+2B(g)![]() C(g)+D(g),经反应5 min后,测得C的浓度为0.3mol·L-1 。则下列说法正确的是
C(g)+D(g),经反应5 min后,测得C的浓度为0.3mol·L-1 。则下列说法正确的是
A. 5 min 内D的平均反应速率为0.02 mol·L-1·min-1
B. 第5min时C的反应速率为0.06 mol·L-1·min-1
C. 经5min后,向容器内再加入A,正反应速率变大
D. 平衡状态时,生成1molD时同时生成1molA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,CO和CH4燃烧的热化学方程式分别为
2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890kJ/mol
1molCO和3molCH4组成的混合气体,在相同条件下完全燃烧时,释放的热量为( )
A.2912kJB.2953kJC.3236kJD.3867kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com