
| A、等于2mol/L |
| B、大于2mol/L |
| C、小于2mol/L |
| D、无法确定 |
| n |
| V |
| ||||
|


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、饱和石灰水中加入少量CaO,恢复至室温后溶液的pH不变 |
| B、稀醋酸加水稀释,醋酸电离程度增大,溶液pH减小 |
| C、盐酸中滴加氨水呈中性,溶液中的溶质为氯化铵 |
| D、向沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、它属于置换反应 |
| B、该反应中NH2-是还原产物 |
| C、该反应中NH3被氧化 |
| D、反应中被氧化和被还原的元素都是H元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙酸乙酯中含有少量乙酸 |
| B、乙醇中含有少量乙酸 |
| C、乙酸中含有少量甲酸 |
| D、溴苯中含有少量苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO42-浓度为3mol/L |
| B、Fe3+的质量为28g |
| C、Fe2(SO4)3浓度为1mol/L |
| D、SO42-为0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、②③④ |
| C、②③④⑤ | D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④⑤ | B、①②⑤ |
| C、②③④⑤ | D、①⑥⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
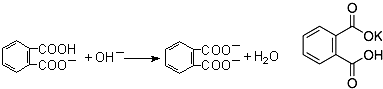
| 实验编号 | 邻苯二甲酸氢钾的质量(g) | 待测NaOH溶液的体积(mL) |
| 1 | 0.4080 | 18.20 |
| 2 | 17.10 | |
| 3 | 16.90 | |
| 4 | 17.00 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com