
废旧碱性锌锰干电池内部的黑色物质A主要含有MnO2、NH4CI、ZnCI2,还有少量的FeCI2和炭粉,用A制备高纯MnCO3,的流程图如下。
(1)碱性锌锰干电池的负极材料是_________(填化学式)。
(2)第Ⅱ步操作的目的是________________________。
(3)第Ⅳ步操作是对滤液a进行深度除杂,除去Zn2+的离子方程式为____________________。 (已知:Ksp(MnS)=2.5×10-13,Ksp(ZnS)=1.6×10-24)
(4)为选择试剂X,在相同条件下,分别用5 g黑色物质M进行制备MnSO4的实验,得到数据如右表:
①试剂x的最佳选择是_________。
②第Ⅲ步中用选出的最佳试剂X与M的
主要成分反应的化学方程式为_________。
(5)第V步系列操作可按以下流程进行:
已知:MaCO3难溶于水和乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH) 2开
始沉淀时pH为7.7。请补充完成以下操作:
操作1:___________________;操作2:过滤,用少量水洗涤2~3次
操作3:检测滤液,表明SO 已除干净; 操作4:___________________;
已除干净; 操作4:___________________;
操作5:低温烘干。
(1)Zn
(2)除去碳和氯化铵
(3)Zn2++MnS= Zn2++MnS+Mn2+
(4)①30%过氧化氢 ②MnO2+H2O2+H2SO4= MnSO4+2H2O+O2↑
(5)加入碳酸钠,控制pH小于7.7
用少量无水乙醇洗涤2——3次
解析试题分析:(1)锌是活泼金属,电池反应中失去电子为负极;(2)加热灼烧碳生成二氧化碳除去,氯化铵分解除去,所以加热的目的是除去碳和氯化铵;(3)该反应是沉淀的转化,沉淀向溶度积小的物质转化,根据溶度积常数MnS不溶, ZnS更难溶;(4)①相同量的M实验4制备得到MnSO4的量最多,所以选用双氧水实验效果做好;②二氧化锰生成硫酸锰,化合价降低为氧化剂,所以双氧水为还原剂产物为氧气,MnO2+H2O2+H2SO4= MnSO4+2H2O+O2↑;(5)反应是制备碳酸锰,所以应加入碳酸钠等可溶性碳酸盐或碳酸氢盐,并调节pH小于7.7(防止生成氢氧化锰),生成碳酸锰,用水洗涤后沉淀表面有水在干燥时易被空气氧化,沉淀不溶于乙醇,且乙醇易挥发易于干燥,所以采用乙醇冲洗除去沉淀表面的水,一般操作2——3次。
考点:考查实验操作与原理有关问题。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
V2O5是接触法制硫酸的重要催化剂,工业上生产V2O5的工艺流程如下:请回答下列问题:
(1)步骤①所得废渣的成分是 (写化学式),它与NaOH溶液反应的离子反应方程式为 。
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):
R2(SO4)n(水层)+2nHA(有机层) 2RAn(有机层)+nH2SO4(水层),
2RAn(有机层)+nH2SO4(水层),
①实验室中步骤②、③使用的主要仪器是 。
②中萃取时必须加入适量碱,其原因是 。
(3)步骤③中X试剂为 ,步骤④的目的是 ,步骤⑤的离子方程式为 。
(4)该工艺流程中,可以循环利用的物质有 和 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
有一无色透明溶液,欲确定是否含有下列离子: Fe2+、Mg2+、Al3+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-,取该溶液进行实验:
| 实验步骤 | 实验现象 |
| (1)取少量该溶液,加几滴紫色石蕊试液 | 溶液变红 |
| (2)取少量该溶液加热,加Cu片和浓H2SO4,加热 | 有无色气体产生,气体遇空气变成红棕色 |
| (3)取少量该溶液,加BaCl2溶液 | 有白色沉淀 |
| (4)取(3)中上层清液,加AgNO3溶液 | 有白色沉淀,且不溶于稀HNO3 |
| (5)取少量该溶液,加NaOH溶液 | 有白色沉淀,NaOH过量时沉淀部分溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
工业上常用含少量Al2O3的钒铁矿(FeO·V2O5)碱熔法提取V2O5。简要流程如下:
已知:①焙烧时Al2O3和V2O5都能与纯碱反应,生成相对应的钠盐,同时放出CO2气体
②常温下物质的溶解度:NaVO3~21.2g/l00g水;HVO3~0.008g/l00g水
请回答:(1)请写出钒铁矿焙烧时,V2O5与纯碱反应化学方程式____ 。
“浸出渣B”的主要成分可能是① ;②_ ___ ;③_ ___;④____ 。(写化学式,可不填满)
(2)生产中,不直接用H2SO4浸泡“烧渣A”获取HVO3的原因是____ 。
(3)“操作①”包括 、洗涤、干燥。如果不洗涤,则产品中可能含有的金属阳离子是 、 。下列装置(部分夹持仪器省去)可用在实验室进行“操作②”的是____ 。(填序号)
(4)NaVO3用于原油的脱硫技术,由V2O5溶于热NaOH溶液中制取,反应的离子方程式为____ 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧化锌[含有Fe(Ⅱ)、Mn(Ⅱ)、Ni(Ⅱ)等杂质]的流程如下: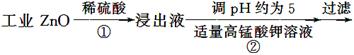
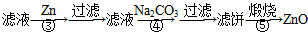
提示:在本实验条件下,Ni(Ⅱ)不能被氧化;高锰酸钾的还原产物是MnO2。
回答下列问题:
(1)反应②中除掉的杂质离子是__________,发生反应的离子方程式为__________;在加高锰酸钾溶液前,若pH较低,对除杂的影响是________________。
(2)反应③的反应类型为____________,过滤得到的滤渣中,除了过量的锌外还有______________。
(3)反应④形成的沉淀要用水洗,检验沉淀是否洗涤干净的方法是________________。
(4)反应④中产物的成分可能是ZnCO3·xZn(OH)2,取干燥后的滤饼11.2 g,煅烧后可得到产品8.1 g,则x等于__________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
二氧化锰可用作干电池去极剂,合成工业的催化剂和氧化剂,玻璃工业和搪瓷工业的着色剂、消色剂、脱铁剂等。
(1)二氧化锰在酸性介质中是一种强氧化剂,请用化学方程式证明:______________________。
(2)锌—锰碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。电池的总反应式为Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)。
①电池工作时,MnO2发生________反应。
②电池的正极反应式为________。
(3)工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下: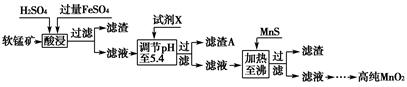
已知:软锰矿的主要成分为MnO2,还含Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物,部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表。
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 |
| 沉淀物 | Zn(OH)2 | CuS | ZnS | MnS | FeS |
| pH | 8.0 | -0.42 | 2.5 | 7 | 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
工业利用精炼镁渣(含有MgO、KCl、MgCl2、BaCl2、CaCl2、FeCl3等杂质)回收MgCl2的工业流程如下:
已知:25 ℃时有关物质的溶度积如下:
| 物质 | CaCO3 | MgCO3 | BaCO3 | Mg(OH)2 | Fe(OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 5.1×10-9 | 5.61×10-12 | 2.64×10-38 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:
(1)溴在周期表中位于 周期 族。
(2)步骤①中用硫酸酸化可提高Cl2的利用率,理由是
(3)步骤④利用了SO2的还原性,反应的离子方程式为
(4)步骤⑥的蒸馏过程中,温度应控制在80~90 ℃,温度过高或过低都不利于生产,请解释原因 。
(5)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的密度相差很大的特点进行分离。分离仪器的名称是 。
(6)步骤①、②之后并未直接用“含Br2的海水”进行蒸馏得到液溴,而是经过“空气吹出”“SO2吸收”“氧化”后再蒸馏,这样操作的意义是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下面是提纯大理石(主要杂质是氧化铁)的流程图:
按要求回答下列问题:
(1)在工业生产中,将块状大理石磨成粉末,并在反应池中安装搅拌机。目的是________。由滤液B得到晶体B,操作过程包括___________(填操作名称)、冷却结晶。
(2)操作Ⅱ中A物质最好应选择___________(填化学式),在该过程中要随时测定pH,在实验室中用pH试纸测定溶液pH的操作是______________________________。
(3)检验Fe3+已完全生成Fe(OH)3沉淀的方法是________________________________。
(4)写出大理石溶解时,发生反应的离子方程式_______________;_________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com