
| A、1mol Cl2与足量Fe反应,转移的电子数为3NA |
| B、分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g |
| C、46g NO2和N2O4混合气体含有原子数为3NA |
| D、常温下,0.1mol/L的NH4NO3溶液中氮原子数为0.2NA |
| 46g |
| 46g/mol |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
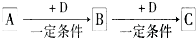 已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系:
已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解水时,加少量硫酸可使电解速率加快 |
| B、H2O2中加入少量MnO2,即可迅速放出气体 |
| C、在木炭粉中加入微量氯酸钾,燃烧时极为剧烈 |
| D、用锌与稀硫酸反应制备氢气时,加入少量硫酸铜加快反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠钾合金可用于快中子反应堆作热交换剂 |
| B、镁燃烧发出耀眼的白光,常用于制造信号弹和焰火 |
| C、铜化学性质不活泼,故古代用作铸币材料 |
| D、铝和Fe2O3混合物在常温下会发生剧烈反应,可以用于野外焊接钢轨 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等体积、等物质的量浓度的NaCl(aq)离子总数大于NaClO(aq)中离子总数 |
| B、pH=3的硫酸溶液中水的电离程度等于pH=11的氨水溶液中水的电离程度 |
| C、0.1 mol/L的NaHA溶液pH=5,则溶液:c(HA-)>c(H+)>c(A2-)>c(H2A) |
| D、向NH4HSO4溶液中滴加NaOH溶液至中性,所得混合液:c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| 实验方案 | 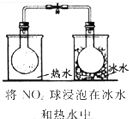 |
 |
 |
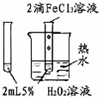 |
| 实验目的 | 探究温度对平衡的影响 2NO2→N2O4 |
比较HCl、H2CO2和 H2SiO3的酸性强弱 |
除去CO2气体中混有的SO2 | 验证FeCl3对H2O2分解反应有催化作用 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、34g H2O2中含有的阴离子数为NA |
| B、标准状况下,22.4L O2作氧化剂时转移电子数一定为4NA |
| C、T℃时,1L pH=6纯水中,含10-6NA个OH- |
| D、10L 0.1mol?L-1的Na2CO3溶液中,Na+、CO32-总数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com