
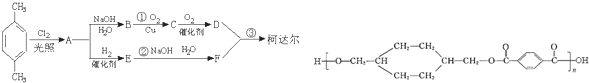
 ;D
;D ;E
;E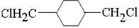
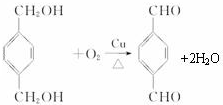 ,反应类型氧化反应
,反应类型氧化反应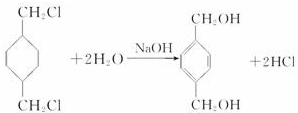 ,反应类型取代反应
,反应类型取代反应 +
+ $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$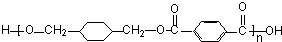 +(2n-1)H2O,反应类型缩聚反应.
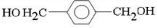
+(2n-1)H2O,反应类型缩聚反应. 分析 由柯达尔的结构式可知,合成其单体为 、
、 ,A通过水解反应生成B,B氧化得到C,C继续被氧化得到D,则B的结构简式为
,A通过水解反应生成B,B氧化得到C,C继续被氧化得到D,则B的结构简式为 ,C为
,C为 ,D为
,D为 ;对二甲苯和氯气发生取代反应生成A为
;对二甲苯和氯气发生取代反应生成A为 ,故F为
,故F为 ,A通过和氢气加成得到E,则E的结构简式为
,A通过和氢气加成得到E,则E的结构简式为 ,E水解得到F,据此进行解答.
,E水解得到F,据此进行解答.
解答 解:由柯达尔的结构式可知,合成其单体为 、
、 ,A通过水解反应生成B,B氧化得到C,C继续被氧化得到D,则B的结构简式为
,A通过水解反应生成B,B氧化得到C,C继续被氧化得到D,则B的结构简式为 ,C为
,C为 ,D为
,D为 ,对二甲苯和氯气发生取代反应生成A为
,对二甲苯和氯气发生取代反应生成A为 ,故F为
,故F为 ,A通过和氢气加成得到E,则E的结构简式为
,A通过和氢气加成得到E,则E的结构简式为 ,E水解得到F,
,E水解得到F,
(1)由上述发信息可知,B为 ,D为
,D为 ,E为
,E为 ,
,
故答案为: ;
; ;
; ;
;
(2)B→C的反应方程式为: ,该反应为氧化反应;
,该反应为氧化反应;
E→F的反应方程式为: ,该反应为取代反应;
,该反应为取代反应;
D+F→柯达尔的反应方程式为: +
+ $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$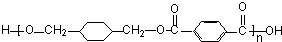 +(2n-1)H2O,该反应为缩聚反应,
+(2n-1)H2O,该反应为缩聚反应,
故答案为: 氧化反应;
氧化反应; 取代反应;
取代反应; +
+ $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$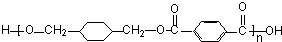 +(2n-1)H2O 缩聚反应.
+(2n-1)H2O 缩聚反应.
点评 本题考查有机物推断,题目难度中等,注意利用柯达尔的结构式确定其单体,结合反应条件,利用逆推法推断,熟练掌握常见有机物结构与性质为解答关键.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| A. | 物质的量浓度为1 mol/L的CuCl2溶液中,含有Cl- 个数为2NA | |
| B. | 若3.01×1023个X原子的质量为8g,则X3气体的摩尔质量是48g/mol | |
| C. | 用特殊方法把固体物质加工到纳米级(1nm~100nm) 的超细粉末粒子,制得纳米材料,纳米材料也是一种胶体 | |
| D. | 在反应2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O中,Cl2 既是氧化剂又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠和镁分别与冷水反应,判断钠和镁金属性强弱 | |
| B. | 在MgCl2与AlCl3溶液中分别加入过量的氨水,判断镁与铝的金属性强弱 | |
| C. | 硅酸钠溶液中通入CO2产生白色沉淀,判断碳酸与硅酸的酸性强弱 | |
| D. | Br2与I2分别与足量的H2反应,判断溴与碘的非金属性强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 化合物 | HCl | NaOH | Cu2(OH)2SO4 | FeSO4•7H2O |
| 氧化物 | H2O | Na2O | CO | Fe3O4 |
| 电解质 | 浓盐酸 | 纯碱 | 胆矾溶液 | 铁 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com