
火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水,将这二种物质混合时可发生如下反应:N2H4+2 H2O2 N2+4H2O,已知0.4 mol液态肼和足量的液态双氧水反应,生成氮气和水蒸汽,放出256.6kJ的热量。
N2+4H2O,已知0.4 mol液态肼和足量的液态双氧水反应,生成氮气和水蒸汽,放出256.6kJ的热量。
(1)反应的热化学方程式为_________________________________________________。
(2)又已知:H2O(l) H2O(g);ΔH=+44 kJ/mol。则16 g液态肼和足量的液态双氧水反应生成液态水时放出的热量是_______________kJ。
H2O(g);ΔH=+44 kJ/mol。则16 g液态肼和足量的液态双氧水反应生成液态水时放出的热量是_______________kJ。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有很大的优点是
(4) 事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计
成原电池的是 。
A.C(s)+H2O(g)=CO(g)+H2(g) △H>0
B.NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) △H<0
C.2H2(g)+O2(g)=2H2O(1) △H<0
以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其负极反应为
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案科目:高中化学 来源: 题型:
在一定条件下发生反应:2A(g)+2B(g) xC(g)+2D(g),在2L密闭容器中,把4molA和
xC(g)+2D(g),在2L密闭容器中,把4molA和
2molB混合,2min后达到平衡时生成1.6molC,又测得反应速率V(D)=0.2mol·L-1·min-1,
下列说法正确的是
A.A和B的转化率均是20% B.x = 4
C.平衡时A的物质的量为2.8mol D.平衡时气体压强比原减小
查看答案和解析>>
科目:高中化学 来源: 题型:
取含有 0.02 mol 的硫酸溶液,先投入 0.24 g 镁粉,再滴入NaOH 溶液,当使溶液中的
镁离子全部转化为沉淀时, 需要NaOH的物质的量为
A.0.02 mol B.0.03 mol C.0.04 mol D.0.01 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示是Zn和Cu(稀硫酸)形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是 ( )
| ① Cu为负极,Zn为正极 ② H+向负极移动 ③ 电子的流动方向是:Zn→Cu ④ Cu极上有H2产生 ⑤ 若有1mol电子流经导线,则可产生0.5mol H2气体 ⑥ 正极反应式:Zn-2e-===Zn2+ |
A.①②③ B.③④⑤
C.④⑤⑥ D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实能说明乙酸(CH3COOH) 属于弱酸的是 ( )
① 1mol/L CH3COOH的 pH=2 ②乙酸能与水以任意比互溶
③ 20mL 1mol/L CH3COOH 与20mL 1mol/LNaOH恰好中和
④ CH3COONa溶液的pH>7
A.①② B.②③ C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
氯化亚铜(CuCl)是重要的化工原料。国家标准规定合格的CuCl产品的主要质量指标为
CuCl的质量分数大于96.5%。工业上常通过下列反应 制备CuCl:2CuSO4+Na2SO3+
制备CuCl:2CuSO4+Na2SO3+
2NaCl+Na2CO3===2CuCl↓+3Na2SO4+CO2↑
(1)CuCl制备过程中需要配制质量分数为20.0%的CuSO4溶液,试计算配制该溶液所需的Cu SO4·5H2O与H2O的质量之比。
SO4·5H2O与H2O的质量之比。
(2)准确称取所制备的0.250 0 g CuCl样品置于一定量的0.5 mol·L-1FeCl3溶液中,待样品完全溶解后,加水20 mL,用0.100 0 mol·L-1Ce(SO4)2溶液滴定到终点,消耗24.60 mL Ce(SO4)2溶液。有关反应的离子方程式为
Fe3++CuCl===Fe2++Cu2++Cl-
Ce4++Fe2+===Fe3++Ce3+
通过计算说明上述样品中CuCl的质量分数是否符合标准。
查看答案和解析>>
科目:高中化学 来源: 题型:
设 NA为阿伏伽德罗常数的值。下列说法正确的是
NA为阿伏伽德罗常数的值。下列说法正确的是
A.1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA
B.0.1mol丙烯酸中含有双键的数目为0.1NA
C.标准状况下,11.2L苯中含有分子的数目为0.5NA
D.在 过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA
过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
把氯气通入浓氨水中,会立即发生下列反应:3Cl2+8NH3·H2O= ==6NH4Cl+N2+8H2O。在标准状况下,把1.12 L Cl2、N2的混合气体(90% Cl2和10% N2,均为体积分数)通过浓氨水,实验测得逸出气体体积为0.672 L(其中有50% Cl2和
==6NH4Cl+N2+8H2O。在标准状况下,把1.12 L Cl2、N2的混合气体(90% Cl2和10% N2,均为体积分数)通过浓氨水,实验测得逸出气体体积为0.672 L(其中有50% Cl2和 50% N2),此反应中被氧化的NH3的质量为 ( )
50% N2),此反应中被氧化的NH3的质量为 ( )
A.3.4 g B.0.34 g
C.1.36 g D.4.48 g
查看答案和解析>>
科目:高中化学 来源: 题型:
由黄铜矿(主要成分是CuFeS2) 炼制精铜的工艺流程示意图如下:
炼制精铜的工艺流程示意图如下:
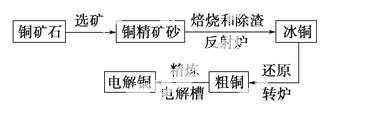
(1)在反射炉中,把铜精矿砂和石英砂混合加热到1 000 ℃左右,黄铜矿与空气反应生成Cu和Fe的低价硫化物,且部分Fe的硫化物转变为低价氧化物。该过程中两个主要反应的化学方程式分别是____________________、__________________________,反射炉内生成 炉渣的主要成分是________;
炉渣的主要成分是________;
(2)冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%~50%。转炉中,将冰铜加熔剂(石英砂)在1 200 ℃左右吹入空气进行吹炼。冰铜中的Cu2S被氧化成Cu2O,生成的Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程发生反应的化学方程式分别是____________;
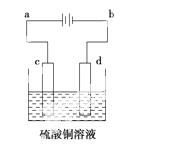
(3)粗铜的电解精炼如右图所示。在粗铜的电解过程中,粗铜板应是图中电极________(填图中的字母);在电极d上发生的电极反应式为____________________________;若粗铜中还含有Au、Ag、Fe,它们在电解槽中的存在形式和位置为____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com