
【题目】下列有关物质性质的应用正确的是
A. 氯化钠溶液显中性,可用铝制容器贮存氯化钠溶液
B. 碳酸钠溶液显碱性,可用热的纯碱溶液除去金属器件表面油污
C. 氮气化学性质通常不活泼,可将炽热的镁粉可放在氮气中冷却
D. 铜的金属性比铁弱,可将海轮浸水部分镶上铜锭以减缓船体腐蚀
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】实验室用溴和苯反应制取溴苯,得到粗溴苯后,要用如下操作精制:①蒸馏;②水洗;③用干燥剂干燥;④用质量分数为10%的NaOH溶液洗。正确的操作顺序是()
A. ①②③①② B. ②④②③① C. ④②③①② D. ②④①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醇酸树脂合成技术成熟、原料易得、涂膜的综合性能良好,是涂料用合成树脂中用量最大、用途最广的品种之一,新型环保醉酸树脂的合成线路如图所示:

(1)E的化学名称是______, D中官能团的名称是____________。
(2)反应①的有机反应类型是_________。
(3)下列说法正确的是_________(填字母编号)。
a.化合物A的核磁共振氢谱有3组峰
b.油脂、蔗糖、麦芽糖酸性水解都能得到2种物质
c. 检验B中所含官能团时,加试剂的顺序依次是过氢量氧化钠溶液、硝酸银溶液
d. 1molC 与足量的银氨溶液反应能生成4 mol Ag
e. 1molE 与足童的金属钠反应产生33.6L H2 (标准状况下)
(4)写出C![]() D的化学方程式:_________。
D的化学方程式:_________。
(5)在Cu 作催化剂,F(C8H10O2)与O2生成C,则F的同分异构体中,符合下列条件的芳香族化合物的结构简式有___________。
a.遇FeCl3溶液发生显色反应;
b.发生消去反应后生成的化合物核磁共振氢谱有5组峰;
(6)已知:RCH3CH=CH2![]() RCHClCH=CH2。上述合成路线,以2-丙醇为原料(无机试剂任选),设计制备OHC-CH2-CHO的合成路线___________。
RCHClCH=CH2。上述合成路线,以2-丙醇为原料(无机试剂任选),设计制备OHC-CH2-CHO的合成路线___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将二氧化硫通入下列试剂,能依次证明SO2具有还原性、漂白性、氧化性、酸性氧化物性质的是( )
①溴水 ②品红溶液 ③酸性高锰酸钾溶液 ④硝酸钡溶液 ⑤含酚酞的氢氧化钠溶液
⑥氢硫酸 ⑦紫色石蕊试液 ⑧氯化铁溶液
A. ①⑤⑥④ B. ⑧②⑥⑤ C. ③⑦⑥⑤ D. ④②⑤①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是重要的化工原料和燃料。将CO2与含少量CO的H2混合,在恒容密闭容器中发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+ H2O(g),图1是在两种投料比[c(CO2)/c(H2+ CO)]分别为1:4和1:6时,CO2平衡转化率随温度变化的曲线, 图2是生成的甲醇/过氧化氢燃料电池的工作原理示意图
CH3OH(g)+ H2O(g),图1是在两种投料比[c(CO2)/c(H2+ CO)]分别为1:4和1:6时,CO2平衡转化率随温度变化的曲线, 图2是生成的甲醇/过氧化氢燃料电池的工作原理示意图
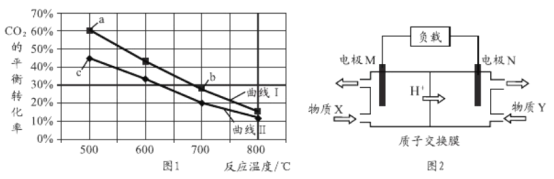
下列有关说法正确的是
A. 图1中b点对应的平衡常数K值大于c点
B. 图1中a点对应的H2的转化率等于30%
C. 图2中电极M上发生还原反应
D. 图2中电极N的反应式: H2O2 +2e- + 2H+= 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与用途对应关系正确的是
A. 明矾易溶于水,可用作净水剂 B. HClO显酸性,可用于杀菌消毒
C. SO2具有氧化性,可用于纸浆漂白 D. 铁粉具有还原性,可用作食品抗氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质分类的正确组合是( )
选项 | 混合物 | 纯净物 | 单质 | 电解质 |
A | 盐酸 | NaOH | 石墨 | K2SO4溶液 |
B | 空气 | Fe(OH)3胶体 | 铁 | Na2CO3 |
C | CuSO4·5H2O | CaCl2 | 水银 | 铜 |
D | 氯水 | KNO3晶体 | O3 | NaCl |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的贮存方法错误的是( )
A. 氢氟酸保存在塑料瓶中
B. 保存氯化亚铁溶液时,要向其中加入少量盐酸和铁粉
C. 少量的锂、钠均保存在煤油中
D. 液氯贮存在干燥的钢瓶里
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法正确的是
A. 在标准状况下,以任意比例混合的CH4与CO2的混合物22.4L,所含有的分子数为NA
B. 在标准状况下,NA个H2O 分子所占体积为22.4L
C. 常温常压下, 1mol Cl2与氢氧化钠溶液反应,发生转移的电子数为2NA
D. 常温常压下,28g氮气含有的核外电子数为10 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com