
(16分,每空2分)
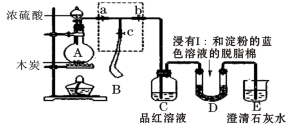
Ⅰ.某课外活动小组为了检验浓硫酸与木炭在加热条件下反应产生的SO2和CO2气体,设计了如图所示实验装置,a、b、c为止水夹,B是用于储气的气囊,D中放有用I2和淀粉的蓝色溶液浸湿的脱脂棉。
请回答下列问题
(1)对于易燃、易爆、有毒的化学物质,往往会在其包装上面贴上危险警告标签。浓硫酸的危险警告标签是

(2)装置A中发生反应的化学方程式为___________________________________。
(3)此实验成败的关键在于控制反应产生气体的速率不能过快,因此设计了虚框部分的装置,则正确的操作顺序是_________________(用操作编号填写)
①向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热;
②待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b;
③打开止水夹a和c,关闭止水夹b;
(4)实验时,装置C中的现象为_______________________________________;
(5)当D中产生_________________现象时,可以说明使E中澄清石灰水变浑浊的是CO2,而不是SO2;
(6)若为检验浓硫酸与木炭在加热条件下生成的水蒸汽,可在装置___________________之间加上一个盛有无水CuSO4的硬质玻璃管。
Ⅱ.Cu与浓硫酸反应可得硫酸铜溶液。某学习小组将铜屑放入一定浓度的硫酸中,加热并不断鼓入空气也可得硫酸铜溶液,其反应原理为2Cu+O2+2H2SO4== 2CuSO4+2H2O。现欲将12.8g铜完全溶解,加蒸馏水后得200 mL溶液。计算:
(7)参加反应的氧气在标准状况下的体积是___________________L。
(8)所得硫酸铜溶液的物质的量浓度是__________________mol/L。
【解析】(16分 每空2分)Ⅰ.(1)C(2)C+2H2SO4(浓) CO2↑+2SO2↑+2H2O;(3)③①②
CO2↑+2SO2↑+2H2O;(3)③①②
(4)品红溶液褪色 (5)进气口一端脱脂棉蓝色变浅,出气口一端脱脂棉蓝色不变
(6)A、B或B、C之间
Ⅱ.(7)2.24L (8)1.0 mol/L
试题分析:Ⅰ.(1)浓硫酸具有强烈的腐蚀性,故应贴腐蚀品的标志,答案C。(2)装置A中浓硫酸有强氧化性,能将C氧化为二氧化碳,反应的化学方程式为C+2H2SO4(浓) CO2↑+2SO2↑+2H2O;(3)先使气体充满B,用B中气体进行试验,答案③①②;(4)产物二氧化硫能使品红溶液褪色,所以装置C中的现象为品红溶液褪色;(5)装置C用于检验SO2的存在, 因SO2 + I2 + 2H2O == H2SO4 + 2HI,所以D为除去SO2并检验已除净,E为检验CO2的存在。进气口一端脱脂棉蓝色变浅,出气口一端脱脂棉蓝色不变,可以说明使E中澄清石灰水变浑浊的是CO2,而不是SO2;(6)产物气体经过溶液会带出水蒸气,所以盛有无水CuSO4的硬质玻璃管应加在C的前面。
CO2↑+2SO2↑+2H2O;(3)先使气体充满B,用B中气体进行试验,答案③①②;(4)产物二氧化硫能使品红溶液褪色,所以装置C中的现象为品红溶液褪色;(5)装置C用于检验SO2的存在, 因SO2 + I2 + 2H2O == H2SO4 + 2HI,所以D为除去SO2并检验已除净,E为检验CO2的存在。进气口一端脱脂棉蓝色变浅,出气口一端脱脂棉蓝色不变,可以说明使E中澄清石灰水变浑浊的是CO2,而不是SO2;(6)产物气体经过溶液会带出水蒸气,所以盛有无水CuSO4的硬质玻璃管应加在C的前面。
Ⅱ.(7)2Cu + O2+2H2SO4====2CuSO4+2H2O
2 1
0.2 x
解得,x=0.1mol,所以参加反应的氧气在标准状况下的体积是0.1mol×22.4mol/L=2.24L;(8)根据铜守衡,CuSO4的物质的量为0.2mol,硫酸铜溶液的物质的量浓度是 =1.0 mol/L。
=1.0 mol/L。
考点:考查浓硫酸的性质。


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源:2014-2015安徽省滁州市六校上高一联考化学试卷(解析版) 题型:填空题
(4分)对于混合物的分离或提纯,常采用的方法有:①过滤、②蒸发、③蒸馏、④萃取、⑤加热分解等。下列各组混和物的分离或提纯应采用什么方法?(填序号)
(1)提取碘水中的碘 ___________
(2)除去食盐溶液中的水 ___________
(3)淡化海水
(4)KCl中含有KClO3
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省东莞市高一上学期期末化学A试卷(解析版) 题型:选择题
化学与社会、生产、生活紧切相关。下列说法正确的是
A.高纯度的硅单质用于制作光导纤维
B.从海水中提取物质都必须通过化学反应才能实现
C.为了增加食物的营养成分,可以大量使用食品添加剂
D.用食醋清洗热水瓶胆内壁附着的水垢(CaCO3)
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高一上学期期末考试化学试卷(解析版) 题型:选择题
下列关于胶体的说法中正确的是
A.胶体能产生丁达尔效应 B.胶体不能通过滤纸
C.胶体外观不均匀 D.胶体不稳定,静置后容易产生沉淀
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高一上学期期末考试化学试卷(解析版) 题型:选择题
下列有关仪器刻度位置的叙述正确的是
A.容量瓶的体积标线刻在瓶颈上
B.量筒的“0”标线在中间
C.量筒最下端刻有“0”标线
D.托盘天平的刻度尺有“0”标线且“0”标在刻度尺的中间
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省广安市高一期末考试化学试卷(解析版) 题型:选择题
有一无色透明溶液,取出少量滴入BaCl2溶液,只有白色沉淀生成;另取一定体积的无色溶液加入过量Na2O2,有无色无味气体产生,同时有白色沉淀生成,其沉淀量与加入Na2O2的量的关系如图所示,根据以上判断在①NH4+ ②H+ ③Al3+ ④Fe2+⑤Mg2+⑥NO3- ⑦CO32-⑧SO42-中一定存在的离子是

A.②③⑤⑧ B.③⑤⑦⑧
C.③④⑤⑧ D.②③⑤⑦⑧
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省广安市高一期末考试化学试卷(解析版) 题型:选择题
下列各组离子,在强酸性溶液中可以大量共存的是
A.K+、Na+、NO3-、SiO32- B.K+、Na+、Ba2+、SO42-
C.K+、Ca2+、Na+、CO32﹣ D.H+、NH4+、K+、Cl-
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省聊城市茌平等三县高二上学期期末联考化学试卷(解析版) 题型:选择题
在pH为4~5的环境中,Cu2+ 、Fe2+ 不能生成沉淀,而Fe3+几乎完全沉淀。工业上制取CuCl2 是将浓盐酸用蒸汽加热到80℃左右,再慢慢加入粗氧化铜(含杂质FeO),充分搅拌使之溶解,欲除去溶液中的杂质离了,下列方法正确的是
A.加入纯Cu将Fe2+ 还原
B.向溶液中加入(NH4)2S 使Fe2+沉淀
C.直接加水加热使杂质离子水解除去
D.在溶液中通入Cl2 ,再加入CuO粉末调节pH为4-5
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省菏泽市高一上学期期末考试化学A试卷(解析版) 题型:选择题
下列对物质的分类正确的是
A.烧碱、纯碱、熟石灰都是碱
B.Na2O、Al2O3、Fe2O3都是碱性氧化物
C.H2SO4、NaOH、NaNO3都是电解质
D.铝土矿、水玻璃、小苏打都是混合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com