
| A. | 11种 | B. | 10种 | C. | 9种 | D. | 8种 |
分析 W蒸气密度是氨气的6倍(相同条件),则W的相对分子质量=17×6=102,取一定量的该有机物完全燃烧,生成CO2和H2O的质量比为22:9,则W分子中C、H原子数目之比=$\frac{22}{44}$:2×$\frac{9}{18}$=1:2,有机物W只含碳、氢、氧三种元素,令有机物W的组成为CnH2nOx,由于W为链状含单官能团的有机物W,则x=1或2,x=1时,n=$\frac{102-16}{14}$=$\frac{43}{7}$,不符合题意,x=2时,n=$\frac{102-16×2}{14}$=5,故W为C5H10O2,为酯,据此书写判断可能结构.
解答 解:W蒸气密度是氨气的6倍(相同条件),则W的相对分子质量=17×6=102,取一定量的该有机物完全燃烧,生成CO2和H2O的质量比为22:9,则W分子中C、H原子数目之比=$\frac{22}{44}$:2×$\frac{9}{18}$=1:2,有机物W只含碳、氢、氧三种元素,令有机物W的组成为CnH2nOx,由于W为链状含单官能团的有机物W,则x=1或2,x=1时,n=$\frac{102-16}{14}$=$\frac{43}{7}$,不符合题意,x=2时,n=$\frac{102-16×2}{14}$=5,故W为C5H10O2,为酯,若为甲酸和丁醇酯化,丁醇有4种,形成的酯有四个:HCOOCH2CH2CH2CH3、HCOOCH2CH(CH3)2、HCOOCH(CH3)CH2CH3、HCOOC(CH3)3;
若为乙酸和丙醇酯化,丙醇有2种,形成的酯有2个:CH3COOCH2CH2CH3、CH3COOCH(CH3)2;
若为丙酸和乙醇酯化,丙酸有1种,形成的酯有1个:CH3CH2COOCH2CH3;
若为丁酸和甲醇酯化,丁酸有2中,形成的酯有2个:CH3CH2CH2COOCH3、(CH3)2CHCOOCH3.
故有9种.故选C.
点评 本题考查有机物分子式确定、同分异构体书写等,关键是利用有机物为单官能团确定O原子数目,难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
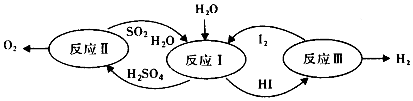
| A. | 设计该循环是为了制取能源气体O2 | |
| B. | 整个循环过程中产生1mol O2的同时产生1molH2 | |
| C. | 图中反应Ⅰ、Ⅱ、Ⅲ均可在常温常压下进行 | |
| D. | 图中反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KClO3═K++3O2-+Cl5+ | B. | NaHCO3═Na++H++CO32- | ||
| C. | H2SO4═H++SO42- | D. | Al2(SO4)3═2Al3++3SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
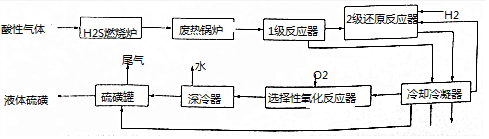
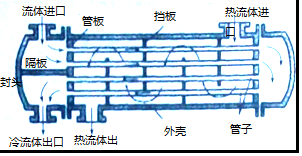
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用分液漏斗分离乙醇与油脂的混合物 | |
| B. | 用玻璃棒蘸取次氯酸溶液点在干燥的pH试纸中部,测定次氯酸溶液的pH | |
| C. | 在含FeCl3杂质的MgCl2溶液中加入适量的MgCO3,微热,充分搅拌,静置,过滤得较纯净的MgCl2溶液 | |
| D. | 将甲烷与氯气按物质的量之比1:2通入烧瓶,光照,制取纯净的CH2Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 231.5mL | B. | 268.8mL | C. | 287.5mL | D. | 313.6mL |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+、K+、Cl-、S2-四种离子的半径依次减小 | |
| B. | 熔融的NaHSO4中阴阳离子的数目比为1:2 | |
| C. | 氢化锂三兄弟--LiH、LiD、LiT三种物质的质子数之比为4:5:6 | |
| D. | 一个乙醛分子中存在7对共用电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com