
| A. | 所用的酸过量 | B. | 生成的盐不水解 | ||
| C. | 酸与碱等物质的量混合 | D. | 反应后溶液中c(A-)=c(M+) |
分析 A.如果酸是强酸,则二者混合溶液呈中性时,酸碱恰好完全反应;
B.如果酸是弱酸,生成的盐为强碱弱酸盐,能水解;
C.如果酸是强酸,混合溶液呈中性时,二者恰好完全反应生成盐,如果是弱酸,要使混合溶液呈中性,则酸要稍微过量;
D.溶液呈中性,则存在c(OH-)=c(H+),再根据电荷守恒判断c(A-)、c(M+)相对大小.
解答 解:A.如果酸是强酸,则二者混合溶液呈中性时,酸碱恰好完全反应,二者的物质的量相等,故A错误;
B.如果酸是弱酸,生成的盐为强碱弱酸盐,能水解,如果酸是强酸,则生成的盐不水解,故B错误;
C.如果酸是强酸,混合溶液呈中性时,二者恰好完全反应生成盐,酸碱的物质的量相等,如果是弱酸,要使混合溶液呈中性,则酸要稍微过量,酸的物质的量大于碱的物质的量,故C错误;
D.溶液呈中性,则存在c(OH-)=c(H+),再根据电荷守恒得c(A-)=c(M+),故D正确;
故选D.
点评 本题考查酸碱混合溶液定性判断,为高频考点,正确判断HA的强弱及生成的盐是否水解是解本题关键,侧重考查学生发散思维能力,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 3.49g | B. | 3.60g | C. | 3.81g | D. | 3.92g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
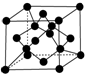 原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子的s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子.
原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子的s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子.| 氟化物 | G的氟化物 | Q的氟化物 | R的氟化物 |
| 熔点/K | 993 | 1 539 | 183 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-丁烯与HBr发生加成反应 | |
| B. | 3-氯戊烷与NaOH乙醇溶液共热发生消去反应 | |
| C. | 甲苯在一定条件下发生溴代反应生成一溴代甲苯的反应 | |
| D. | 邻羟基苯甲酸与NaHCO3溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol CO+2 mol H2O(g)+1 mol CO2+1 mol H2 | |
| B. | 1 mol CO+1 mol H2O(g)+1 mol CO2+1 mol H2 | |
| C. | 0.5 mol CO+1.5 mol H2O(g)+0.4 mol CO2+0.4 mol H2 | |
| D. | 0.5 mol CO+1.5 mol H2O(g)+0.5 mol CO2+0.5 mol H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 体积大小:③>②>① | B. | 原子数目:③>①>② | C. | 密度大小:②>③>① | D. | 质量大小:②>③>① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com