
【题目】A~H均为短周期元素,A~F在元素周期表中的相对位置如下图所示,G与其它七种元素不在同一周期,H是短周期中原子半径最大的主族元素。由B、G组成的气态化合物甲水溶液呈碱性。
A | B | C | |
D | E | F |
请回答下列问题:
(1)写出甲的电子式,实验室制取气体甲的化学方程式为。
(2)B、C、G个数比为1:1:5形成的化合物的化学键类型为。
A.离子键
B.极性键
C.非极性键
(3)请用电子式表示AE2的形成过程。
(4)用离子符号表示C、E、F、H四种离子的半径由大到小的顺序。
(5)用一个离子方程式解释A比D非金属性强的原因。
【答案】(1)![]() 2NH4Cl+Ca(OH)2
2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
(2)b
(3)![]()
(4)S2->Cl->O2->Na+
(5)CO2+H2O+SiO32-=CO32-+H2SiO3(其它合理的也得分)
【解析】试题分析:A~H均为短周期元素,A~F在元素周期表中的相对位置如图所示,G与其它七种元素不在同一周期,H是短周期中原子半径最大的主族元素,则H是Na。由B、G组成的气态化合物甲水溶液呈碱性,该化合物是氨气,则B是N,G是H,A是C,C是O,D是Si,E是S,F是Cl。
(1)氨气是共价化合物,电子式为![]() ,实验室制取气体氨气的化学方程式为2NH4Cl+Ca(OH)2
,实验室制取气体氨气的化学方程式为2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O。(2)B、C、G个数比为1:1:5形成的化合物是一水合氨,其中含有的化学键类型为极性键,答案选b。(3)用电子式表示CS2的形成过程为
CaCl2+2NH3↑+2H2O。(2)B、C、G个数比为1:1:5形成的化合物是一水合氨,其中含有的化学键类型为极性键,答案选b。(3)用电子式表示CS2的形成过程为![]() 。
。
(4)离子的核外电子层数越多,离子半径越大,核外电子排布相同时离子半径随核电荷数的增大而减小,则C、E、F、H四种离子的半径由大到小的顺序为S2->Cl->O2->Na+。(5)较强酸制备较弱酸可以说明非金属性强弱,则用离子方程式解释A比D非金属性强的原因为CO2+H2O+SiO32-=CO32-+H2SiO3。


科目:高中化学 来源: 题型:
【题目】用双线桥标出下列反应中电子转移的方向和数目,并填空。
(1)Cl2+SO2+2H2O=H2SO4+2HCl
氧化剂是__________;被氧化的物质是_____________
(2)3NO2+2H2O=2HNO3+NO
氧化产物是___________.氧化剂与还原剂的质量比为_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是
A.1mol羟基与1mol氢氧根离子所含的电子数均为9NA
B.常温下,44g N2O和CO2组成的混合气体,所含原子数为3NA
C.0.1mol/L的NaClO溶液,含有的阴离子数为0.1NA
D.常温下,将1molFe投入过量浓硝酸中,转移的电子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在周期表中1-36号之间的W、X、Y、Z、Q六种元素,它们的原子序数依次增大,已知W与其余五种元素既不同周期也不同主族,X原子的L层p轨道中有2个电子,Y元素原子的最外层有3个自旋方向相同的未成对电子,Z元素原子基态时,核外电子排布在3个能级上,且有2个未成对电子,Q元素在第四周期,原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态。
(1)按电子排布,Q元素在周期表中属 区。
(2)第一电离能Y Z,电负性Y Z(填“>”“<”或“=”)。
(3)W与Z形成的常见化合物有W2Z、W2Z2,W与Y能形成多种二元化合物,如YW3、Y2W4、Y3W5、Y4W6……,W2Z分子中Z原子的杂化类型为 ,YW3分子的立体构型为 ,YW3极易溶于W2Z的主要原因有 。
(4)若向含有Q2+的硫酸盐溶液中滴加过量氨水,得到深蓝色溶液后再加乙醇,有深蓝色晶体析出,该晶体阳离子中含有的化学键有 。
(5)Q+与Y3-形成的晶胞结构如图所示。阴、阳离子间的核间距为a pm,阿伏伽德罗常数用NA表示,则晶体的密度为 g/cm3.
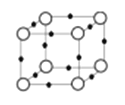
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活中的某些问题常常涉及化学知识,下列叙述错误的是( )
A.纯碱可制造玻璃,也可除去物品表面的油污
B.用聚氯乙烯代替木材生产包装盒、快餐盒等,以减少木材的使用
C.黄河入海口沙洲的形成和卤水点豆腐,都体现了胶体聚沉的性质
D.“煤改气(电)”等改造工程有利于减少环境污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种白色粉末是无水碳酸钠和碳酸氢钠的混合物,称取4.42g灼烧至恒重,把放出的气体通入足量澄清石灰水中,生成2.00g沉淀,灼烧后的残渣能与30mL盐酸恰好完全反应。试求:
(1)该白色粉末灼烧后产生气体在标准状况下的体积?
(2)原混合物中各物质的质量。
(3)所用盐酸的物质的量浓度。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)将等物质的量的A和B,混合于2 L的密闭容器中,发生如下反应:3A(g) + B(g) ![]() xC(g) +2D(g),5min后测得c(D)=0.5mol·L-1,c(A)∶c(B)=3∶5,C的反应速率是0.1mol·L-1·min-1。
xC(g) +2D(g),5min后测得c(D)=0.5mol·L-1,c(A)∶c(B)=3∶5,C的反应速率是0.1mol·L-1·min-1。
①A在5min末的浓度是____________。
②v(B)=____________。
③x=____________。
(2)在25℃时,向100mL含氯化氢14.6g的盐酸溶液中,放入5.6g纯铁粉,反应进行到2min末收集到氢气1.12 L(标准状况),在此后又经过4min,铁粉完全溶解。若不考虑溶液体积的变化,则:
①前2min内用FeCl2表示的平均反应速率是______________。
②后4min内用HCl表示的平均反应速率是________________。
③前2min与后4min相比,反应速率__________较快,其原因是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的浓度的说法正确的是
A.将5.85 g NaCl固体溶于1 L水中可配成0.1mol/L的NaCl 溶液
B.500 ml 0.5mol/L 的NaOH溶液含NaOH分子0.25 mol
C.把200mL 3mol/L的BaCl2溶液跟100mL 3mol/L的KCl溶液混合后,溶液中的c(Cl-)仍然是3mol/L(忽略混合后体积变化)
D.把100g 20%的NaCl溶液跟100g H2O混合后,NaCl溶液的质量分数是10%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇被称为2l世纪的新型燃料,工业上通过下列反应①和②,用CH4和H2O为原料来制备甲醇。
① CH4(g)+H2O(g) ![]() CO(g)+3H2(g) ΔH1
CO(g)+3H2(g) ΔH1
② CO(g)+2H2(g) ![]() CH3OH(g) ΔH2
CH3OH(g) ΔH2
将0.20mol CH4(g)和0.30 mol H2O(g)通入容积为10L的密闭容器中,在一定条件下发生反应①,达到平衡时,CH4的转化率与温度、压强的关系如图。
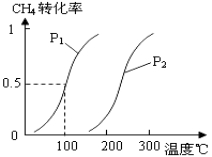
(1)温度不变,缩小体积,增大压强,①的反应速率 ______(填“增大”、“减小”或“不变”),平衡向 ___方向移动。
(2)温度升高,反应①的ΔH1 0(填“<”、“=”或“>”),其平衡常数表达式为K= ,100℃时的平衡常数值是 ______。
(3)在压强为0.1 MPa条件下, 将a mol CO与 3 a mol H2的混合气体在催化剂作用下进行反应②生成甲醇。为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。请在下表空格中填入剩余的实验条件数据。
实验编号 | T(℃) | n (CO)/n(H2) | P(MPa) |
I | 150 | 1/3 | 0.1 |
II | 5 | ||
III | 350 | 5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com