
| A. | 石墨不如金刚石稳定 | |
| B. | 金刚石和石墨互为同位素 | |
| C. | 石墨能量高于金刚石 | |
| D. | 等质量的金刚石与石墨完全燃烧,石墨放出的能量少 |
分析 12g石墨完全转化成金刚石时需要吸收E kJ的能量,说明石墨的能量低于金刚石的能量,石墨更稳定,金刚石的能量高,等质量石墨和金刚石完全燃烧时释放的能量金刚石比石墨多.
解答 解:A、石墨转化为金刚石要吸收能量,说明石墨的能量低,石墨比金刚石稳定,故A错误;
B、金刚石与石墨是由碳元素组成的物理性质不同的单质,互为同素异形体,故B错误;
C、石墨转化为金刚石要吸收能量,说明石墨的能量低于金刚石,故C错误;
D、金刚石的能量高,等质量的石墨和金刚石完全燃烧时释放的能量金刚石比石墨多,石墨放出的能量少,故D正确.
故选D.
点评 本题考查金刚石和石墨的转化以及涉及到的能量变化,注意能量低的物质更稳定即可解答.


科目:高中化学 来源: 题型:选择题
| A. | ①②③⑥ | B. | ②④⑥ | C. | ③⑤⑥⑦ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠着火,不能用泡沫灭火器扑火 | |
| B. | 实验台上的酒精灯碰翻着火,立即用湿抹布扑火 | |
| C. | 皮肤溅上浓硫酸,立即用大量水冲洗 | |
| D. | 汞洒落地面,应立即撒上一层硫磺粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
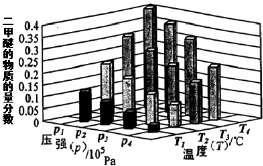
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由Cu、Zn和稀硫酸组成的原电池工作时,若Cu极生成0.2gH2,则电路通过电子0.4NA | |
| B. | 18gD2O中含有的质子数目为10NA | |
| C. | 1molCl2发生反应时,转移的电子数一定是2NA | |
| D. | 常温常压下,16gO3所含的原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性 | |
| B. | 碘水与碘化钾淀粉试纸作用出现蓝色,说明碘具有氧化性 | |
| C. | 往饱和Na2CO3溶液中通入CO2有固体析出,说明NaHCO3溶解度小于Na2CO3 | |
| D. | 同温下,等物质的量浓度的Al2(SO4)3比MgSO4溶液的pH小,说明镁比铝的金属性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
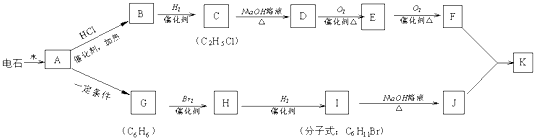
 ;
;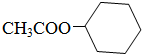 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com