


科目:高中化学 来源: 题型:
A、CaCO3
| ||||||||
B、Cu
| ||||||||
C、KMnO4
| ||||||||
D、NH3
|
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知由C、H、O三种元素组成的化合物A,其相对分子质量为60,且A能与NaHCO3辣反应生成CO2. 请回答下列问题:
已知由C、H、O三种元素组成的化合物A,其相对分子质量为60,且A能与NaHCO3辣反应生成CO2. 请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、所有的电子在同一区域里运动 |
| B、同一原子中,1s、2s、3s所能容纳的电子数越来越多 |
| C、电子云图通常用小黑点来表示电子的多少,黑点密度大,电子数目大 |
| D、能量高的电子在离核远的区域运动,能量低的电子在离核近的区域运动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、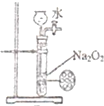 制备少量的氧气 |
B、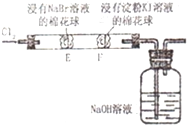 证明氧化性Cl2>Br2>I2 |
C、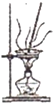 将海带灼烧成灰 |
D、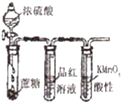 说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、脂肪 | B、乙酸 |
| C、葡萄糖 | D、蛋白质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com