
相同温度下,根据三种酸的电离常数,下列判断正确的是
( )
| 酸 | HX | HY | HZ |
| 电离常数K | 9×10-7 | 9×10-6 | 10-2 |
A.三种酸的强弱关系:HX>HY>HZ
B.反应HZ+Y-===HY+Z-能够发生
C.相同温度下,0.1 mol/L的NaX、NaY、NaZ溶液,NaZ溶液pH最大
D. 相同温度下,1 mol/L HX溶液的电离常数大于0.1 mol/L HX
相同温度下,1 mol/L HX溶液的电离常数大于0.1 mol/L HX
科目:高中化学 来源: 题型:

A.两者互为同分异构体,都是以Pt原子为中心的四面体结构
B.两者互为同分异构体,都是以Pt原子为中心的平面结构
C.两者为同一物质,都是以Pt原子为中心的四面体结构
D.两者为同一物质,都是以Pt原子为中心的平面结构
查看答案和解析>>
科目:高中化学 来源: 题型:
两位同学根据电解原理,利用塑料瓶、9 V电池、大头针进行电解污水的实验。实验装置如下图。

根据上图回答下列问题:
(1)根据电浮选凝聚法处理污水的净化原理写出阳极区和阴极区上各自的电极反应式:
阳极:_________________________________________________;
阴极:______________________________________________。
(2)试分析不能参加反应的污物是如何沉淀的:______________________________________________。
(3)最后悬浮物为什么会形成浮渣:_______________________________________________。
(4)甲同学模拟该原理进行污水处理实验,在电压符合要求的情况下,发现产生气泡速度缓慢,无法使悬浮物形成浮渣。其原因是______________________________________________。
乙同学为甲同学提出一种切实可行的解决措施是向污水中加入适量的__________溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,0.1 mol/L的HA溶液中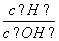 =1010,0.01 mol/L的BOH溶液pH=12。请回答下列问题:
=1010,0.01 mol/L的BOH溶液pH=12。请回答下列问题:
(1)HA是____________(填“强电解质”或“弱电解质”,下同),BOH是____________。
(2)HA的电离方程式是_______________________________________________。
(3)在加水稀释HA的过程中,随着水量的增加而减小的是________(填字母)。
A. B.
B.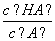
C.c(H +)与c(OH-)的乘积 D.c(OH-)
+)与c(OH-)的乘积 D.c(OH-)
(4)在体积相等、pH相等的HA溶液与盐酸溶液中加入 足量Zn,HA溶液中产生的气体比盐酸中产生的气体________(填“多”、“少”或“相等”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,若HA溶液和NaOH溶液混合后pH=7,下列说法不合理的是( )
A. 反应后HA溶液可能有剩余
反应后HA溶液可能有剩余
B.生成物NaA的水溶液的pH可能小于7
C.HA溶液和NaOH溶液的体积一定相等
D.HA溶液的c(H+)和NaOH溶液的c(OH-)可能不相等
查看答案和解析>>
科目:高中化学 来源: 题型:
据报道,美国正在研究的锌电池可能取代目前广泛使用的铅蓄电池。锌电池具有容量大、污染少等优点。电池反应为2Zn+O2=2ZnO,原料为锌粒、电解液和空气。下列叙述正确的是
A.锌为正极,空气进入负极反应
B.负极反应为Zn+2OH--2e-=ZnO+H2O
C.正极发生氧化反应
D.电解液肯定是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液一定呈中性的是( )
A.c(H+)=c(OH-)=10-6 mol/L的溶液
B.pH=7的溶液
C.使石蕊试液呈紫色的溶液
D.酸与碱恰好完全反应生成正盐的溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com