
 2SO3��g�� ��H����196��6 kJ��mol��1
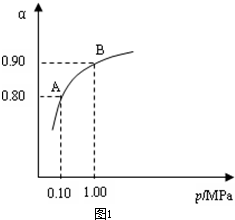
2SO3��g�� ��H����196��6 kJ��mol��1 2SO2+O2 ��550 ��ʱ��ƽ�ⳣ��K=_________�� A��B��ʾ��ͬѹǿ�µ�ƽ��ת���ʣ�ͨ����ҵ�����в��ó�ѹ��ԭ���ǣ�__________________�����Ƚϲ�ͬѹǿ�µ�ƽ�ⳣ����K��0��10 MPa�� _________K��1��0 MPa������ ������������������
2SO2+O2 ��550 ��ʱ��ƽ�ⳣ��K=_________�� A��B��ʾ��ͬѹǿ�µ�ƽ��ת���ʣ�ͨ����ҵ�����в��ó�ѹ��ԭ���ǣ�__________________�����Ƚϲ�ͬѹǿ�µ�ƽ�ⳣ����K��0��10 MPa�� _________K��1��0 MPa������ ������������������ 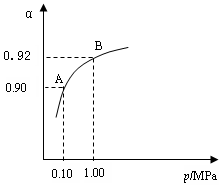
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
| ���� |
| ���� |
| ���� |
| ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
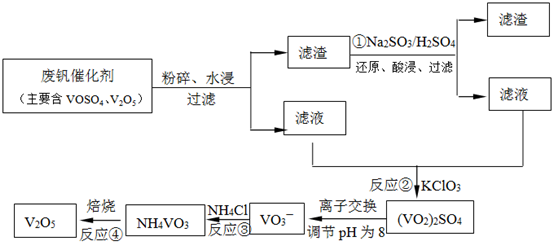
 ��ҵ���Ի�����Ϊԭ������������Ҫ��Ϊ�����ν��У������ա������������գ���ش����и����⣺
��ҵ���Ի�����Ϊԭ������������Ҫ��Ϊ�����ν��У������ա������������գ���ش����и����⣺| ���� | �� |
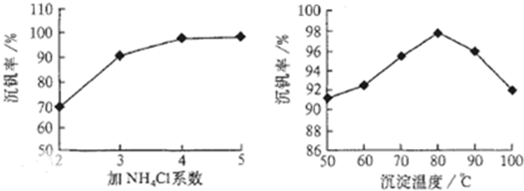
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
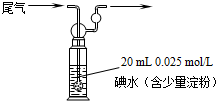
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com