
| △ |
| △ |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 产品B:1,8-二硝基萘
产品B:1,8-二硝基萘 产品B可溶于质量分数大于98%的硫酸,产品A不能.利用这一可以将这两种异构体分离.下列说法正确的是( )
产品B可溶于质量分数大于98%的硫酸,产品A不能.利用这一可以将这两种异构体分离.下列说法正确的是( )| A、可以通过蒸馏的办法分离产品A和产品B |
| B、要获得产品A,将上述硝化产物加入适量的98.3%硫酸,通过萃取获得产品A |
| C、要获得产品B,将上述硝化产物加入适量的98.3%硫酸,充分搅拌,用耐酸漏斗过滤得滤液,向滤液中注水便有产品B析出 |
| D、是否生成两种二硝基物,可以取反应混和物,进行纸层析实验来检验 |
查看答案和解析>>
科目:高中化学 来源: 题型:
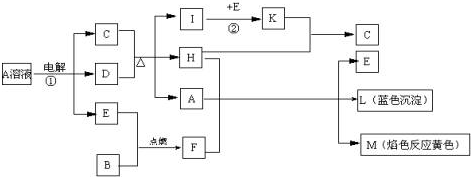
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、③④ | C、②③ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、高纯度的单晶硅用于制造登月车的光电池和光导纤维 |
| B、棉、麻、羊毛及合成纤维完全燃烧都只生成CO2和H2O |
| C、加碘食盐能使淀粉溶液变蓝 |
| D、有些肾病患者要定期进行血透,血透原理是利用渗析的方法净化血液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com