
CuI��һ�ֲ�����ˮ�İ�ɫ���壬�����ɷ�Ӧ��2Cu2++4I��=2CuI��+I2���õ�������ͭƬ��ʯī���缫�����KI��Һ��ȡCuI��Ϊȷ�Ϸ�Ӧ�����ͨ��ǰ����Һ���ּ����������ķ�̪��Һ�͵�����Һ�����һ��ʱ���õ���ɫ������ͬʱ��������Һ��죬��������Һ����������˵����ȷ���� �� ��
��ͭƬ��������ʯī������ ��ͭƬ��������ʯī������
���������������� ����������������
�ݰ�ɫ������������������ �ް�ɫ������������������
����������Һ������ԭ����2Cu+4I�D�D4e��=2CuI��+I2 �������۱���
����������Һ������ԭ����4OH�D�D4e�D=2H2O+O2��O2��I������ΪI2���������۱���
A��ֻ�Тڢܢݢ� B��ֻ�Т٢ܢޢ� C��ֻ�Тڢۢݢ� D��ֻ�Т٢ۢޢ�
 �ƸԴ��ž�ϵ�д�
�ƸԴ��ž�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
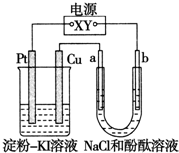 ��2011?�㽭��У����������CuI��һ�ֲ�����ˮ�İ�ɫ���壬�������ɷ�Ӧ��2Cu2++4I-�T2CuI��+I2���õ�����ͼ��ʾװ���У�a��b���Ƕ��Ե缫��ͨ��һ��ʱ����ڵ���-KI��Һ��������Χ����ɫ��������˵����ȷ���ǣ�������
��2011?�㽭��У����������CuI��һ�ֲ�����ˮ�İ�ɫ���壬�������ɷ�Ӧ��2Cu2++4I-�T2CuI��+I2���õ�����ͼ��ʾװ���У�a��b���Ƕ��Ե缫��ͨ��һ��ʱ����ڵ���-KI��Һ��������Χ����ɫ��������˵����ȷ���ǣ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
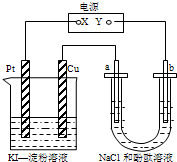 CuI��һ�ֲ�����ˮ�İ�ɫ���壬�������ɷ�Ӧ��2Cu2++4I-=2CuI��+I2���õ�����ͼ��ʾװ���У�a��b���Ƕ��Ե缫��ͨ��һ��ʱ�����KI-������Һ��������Χ����ɫ��������˵����ȷ���ǣ�������
CuI��һ�ֲ�����ˮ�İ�ɫ���壬�������ɷ�Ӧ��2Cu2++4I-=2CuI��+I2���õ�����ͼ��ʾװ���У�a��b���Ƕ��Ե缫��ͨ��һ��ʱ�����KI-������Һ��������Χ����ɫ��������˵����ȷ���ǣ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��08ɽ���߿���̾���CuI��һ�ֲ�����ˮ�İ�ɫ���壬�������ɷ�Ӧ�������������з�Ӧ�Ƶã�2Cu2++4I�D��2CuI��+I2������ʯīΪ��������CuΪ�������KI��Һ��ͨ��ǰ����Һ�м���������̪�͵�����Һ����ʼ���ã���������Һ�ʺ�ɫ������������Һ����ɫ������������Һ����ɫ����ȷ�����ǣ� ��
A��2I����2e�D��I2���������۱���
B��Cuһ2e�D��Cu2+�� Cu2+����Һ����ɫ
C��2Cu2++4I�D��2CuI��+I2���������۱���
D��4OH����4e��=2H2O+O2 O2��I������ΪI2���������۱���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��12�֣�
1.��ͼΪ����������������������ʵ��װ�ã���װ�� ��Zn�缫�ϵĵ缫��ӦΪ �������Zn����Pt��һ��ʱ��������缫������2�λ�ɫK3[Fe(CN)6](���軯��)��Һʱ���ձ��е������� �������ķ�Ӧ�����ӷ���ʽ�� ��
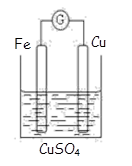
2.CuI��һ�ֲ�����ˮ�İ�ɫ���壬�������ɷ�Ӧ��2Cu2+ + 4I���� 2CuI�� + I2���õ�������ʯīΪ��������CuΪ�������KI��Һ��ͨ��ǰ����Һ�м���������̪�͵�����Һ���ٵ�ʼ���ã�����������ʵ�������� �������ĵ缫��Ӧ�� ��
����������Һ����ɫ��ͬʱ����������� ������������Һ
����ɫ����ȷ������ ��
A. 2I�� �� 2e- = I2 ���������۱���
B. Cu �� 2e- = Cu2+��Cu2+����ɫ
C. 2Cu �� 4I���� 4e-= 2CuI�� + I2�� �������۱���
D. 4OH���� 4e- = 2H2O + O2 ��O2��I������ΪI2���������۱���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com