
| A. | Ar的结构示意图: | B. | CO2的分子模型示意图: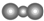 | ||
| C. | CSO的电子式: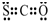 | D. | N2的结构式::N≡N: |
分析 A.Ar原子的核电荷数=核外电子总数=18,最外层为8个电子;
B.二氧化碳分子中,氧原子半径小于碳原子;
C.CSO的结构与二氧化碳相似,分子中存在1个C=S和1个C=O键;
D.氮气分子中存在氮氮三键,结构式中不参与标出未成键电子对.
解答 解:A.Ar的最外层达到8电子稳定结构,其正确的原子结构示意图为: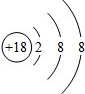 ,故A错误;
,故A错误;
B.二氧化碳为直线型结构,碳原子的原子半径大于氧原子,二氧化碳正确的比例模型为: ,故B错误;
,故B错误;
C.CSO的结构与二氧化碳相似,属于共价化合物,分子中存在1个C=S和1个C=O键,其电子式为: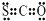 ,故C正确;
,故C正确;
D.氮气的电子式为: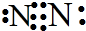 ,将电子式中的共用电子对换成短线,即为氮气的结构式,则氮气正确的结构式为:N≡N,故D错误;
,将电子式中的共用电子对换成短线,即为氮气的结构式,则氮气正确的结构式为:N≡N,故D错误;
故选C.
点评 本题考查常见化学用语的判断,题目难度中等,涉及电子式、离子结构示意图、结构式、比例模型等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生规范答题的能力.


科目:高中化学 来源: 题型:选择题
| A. | c(H+) | B. | Ka(HCOOH) | C. | $\frac{c(HCO{O}^{-})}{c({H}^{+})}$ | D. | $\frac{c({H}^{+})}{c(HCOOH)}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气体的摩尔体积即标准状况下单位物质的量气体的体积 | |
| B. | 温度压强一定的情况下,气体的体积决定于气体的物质的量多少和分子本身的大小 | |
| C. | 配制物质的量浓度的溶液,定容时俯视,配得溶液浓度偏大 | |
| D. | 电解18g水,两极生成的气体体积比约为2:1,质量比2:16 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 应量取浓盐酸体积/mL | 应选用容量瓶的规格/mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①→④→③→② | B. | ①→③→②→④ | C. | ①→③→④→② | D. | ①→②→③→④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| W | X | Y |
| Z |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D、E、F六种元素的原子序数依次增大.已知:F的原子序数为29,其余均为短周 期主族元素;E原子价电子(外围电子)排布式为 msnmpn-1;D原子的最外层电子数为偶数;A、C原子 的P轨道上都有两个未成对电子.请回答下列问题:
A、B、C、D、E、F六种元素的原子序数依次增大.已知:F的原子序数为29,其余均为短周 期主族元素;E原子价电子(外围电子)排布式为 msnmpn-1;D原子的最外层电子数为偶数;A、C原子 的P轨道上都有两个未成对电子.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器内的压强不再变化 | |
| B. | 单位时间内消耗amolA,同时生成3amolC | |
| C. | C生成的速率与C分解的速率相等 | |
| D. | 混合气体的物质的量不再变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com