
ij��Һ�У����ܺ������������е������֣�Cl﹣��Mg2+��Ba2+��CO32﹣��SO42﹣��Na+��ȡ��ͬ���������ݸ���100mL��Һ��������ʵ�飺
��һ�ݼ�����������Һ�г���
�ڶ��ݼ����������Ȼ�����Һ���ó�����8.6g������������ϴ�Ӹ����������Ϊ4.66g����������Һ�м�����������Һ�г������ɣ���������ʵ���жϣ�
��1���϶����ڵ������� ���϶������ڵ������� �����ܴ��ڵ����� ��д��8.6g�����ﱻ�����ܽ�ʱ���������ӷ���ʽ ��
��2��100mL��Һ��Na+�����ʵ���Ϊ mol��
���㣺 ���������ӵļ��飻���������ӵļ��飮
������ �ټ���AgNO3��Һ�г���������˵����Һ�п��ܴ���Cl﹣��CO32﹣��SO42﹣��
��4.66gΪ���ᱵ�����������ʵ���Ϊ0.02mol��8.6gΪ���ᱵ��̼�ᱵ���ݴ˿��Լ����̼�ᱵ�����ʵ�����
�ٸ��ݵ���غ㣬�ó�һ�����������ӣ��ݴ˽����жϣ�
��� �⣺����AgNO3��Һ�г���������������Cl﹣��CO32﹣��SO42﹣��
�ڲ����������4.66g����Ϊ���ᱵ�����ᱵ�����ʵ����ǣ�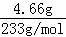 =0.02mol��8.6g���������ᱵ��̼�ᱵ��̼�ᱵ����Ϊ��8.6g﹣4.66g=3.94g��̼�ᱵ���ʵ���Ϊ��
=0.02mol��8.6g���������ᱵ��̼�ᱵ��̼�ᱵ����Ϊ��8.6g﹣4.66g=3.94g��̼�ᱵ���ʵ���Ϊ��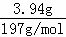 =0.02mol������ԭ��Һ��һ�����ڣ�CO32﹣��SO42﹣�����һ��û����Ba2+��Mg2+������Һ������ԭ���֪��һ������Na+��
=0.02mol������ԭ��Һ��һ�����ڣ�CO32﹣��SO42﹣�����һ��û����Ba2+��Mg2+������Һ������ԭ���֪��һ������Na+��
c��CO32﹣��=c��SO42﹣��=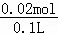 =0.2mol/L���ٸ��ݵ���غ㣬�����Ϊ��n��+��=n��Na+��=0.08mol��
=0.2mol/L���ٸ��ݵ���غ㣬�����Ϊ��n��+��=n��Na+��=0.08mol��
��1���������Ϸ�����֪��ԭ��Һ��һ�����ڵ�������Na+��CO32﹣��SO42﹣��һ��û�е�����Mg2+��Ba2+�����ܴ���Cl﹣��̼�ᱵ�����ᷴӦ�������ᱵ��������̼�����ˮ�����ӷ�Ӧ����ʽΪ��BaCO3+2H+═Ba2++H2O+CO2�����ʴ�Ϊ��Na+��CO32﹣��SO42﹣��Mg2+��Ba2+��Cl﹣��BaCO3+2H+═Ba2++H2O+CO2����
��2��n��Na+��=2n��CO32﹣��+2n��SO42﹣��=0.02��2+0.02��2=0.08mol�������������ӣ���ô�����ӣ�0.08mol���ʴ�Ϊ����0.08��
������ ���⿼�����ӵļ��飬���ö���ʵ��Ͷ�������������ϵ�ģʽ�������˽����Ѷȣ�ͬʱ�漰���ӹ��桢���ӷ�Ӧ�ȶ��ǽ�����ע�����Ϣ��������K+��ȷ���׳���ʧ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��һ�������£�2SO2+O2⇌2SO3��Ӧ��ƽ���SO2��ת����Ϊ45.3%������V2O5����������SO2��ת����Ϊ��������
| �� | A�� | ����45.3% | B�� | С��45.3% | C�� | ����45.3% | D�� | ��ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�±��г���a﹣f����Ԫ�������ڱ�ǰ�����ڵ�λ�ã�
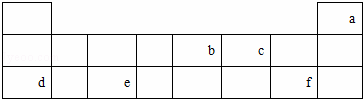
��ش��������⣺
��1��cԪ�ص�����������dԪ��λ��IA�壮
��2����Ԫ�ط��ű�ʾ������Ԫ���У��������ȶ���Ԫ��ԭ�ӽṹʾ��ͼ �� Ԫ�ص�ԭ�Ӱ뾶���
��3���ǽ�����b c��������ڡ���С�ڡ���
��4���û�ѧʽ��ʾ������Ԫ���У��������������������������� ������������Ӧˮ����������ǿ���� 4
��5��д��dԪ�ص�����ˮ��Ӧ�����ӷ���ʽ
��6��д��eԪ�ص�����NaOH��Ӧ�����ӷ���ʽ
��7���õ���ʽ��ʾ������d2c���γɹ��� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ���ǣ���
�ٱ�״���£�6.02��1023��������ռ�����Լ��22.4L
��0.5mol H2��ռ���Ϊ11.2L
�۱�״���£�1mol H2O�����Ϊ22.4L
�ܳ��³�ѹ�£�28g CO��N2�Ļ������������ԭ����Ϊ2NA
�ݸ������������Ħ�������ԼΪ22.4L•mol﹣1
�ޱ�״���£������ͬ������ķ�������ͬ��
A�� �٢ۢ� B�� �ܢ� C�� �ۢܢ� D�� �٢ܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ԭ��Ӧ�У�ˮ�����ÿ���������������ԭ�����������������ǻ�ԭ�����ȷ��������ַǻ�ԭ���ȣ����з�Ӧ��Br2+SO2+2H2O=H2SO2+2HBr��Ƚϣ�ˮ��������ͬ���ǣ���
A�� ���ˮ��2H20=2H2��+O2�� B�� 4Fe��OH��2+O2+2H2O=4Fe��OH��3
C�� 2F2+H2O=4HF+O2 D�� 3NO2+H2O=2HNO3+NO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ݱ������ҹ�ӵ����ȫ������Ȩ������ȼ�ϵ�س����ڰ��˻��ڼ�Ϊ�˶�Ա�ṩ����ij������ȼ�ϵ�صĵ��ҺΪKOH��Һ�������йص�ص���������ȷ���ǣ���
A�� ������ӦʽΪ��O2+2H2O+4e﹣═4OH﹣
B�� ����һ��ʱ����Һ�е�KOH�����ʵ�������
C�� �������Һ�е�OH﹣���ƶ�
D�� �øõ�ص��CuCl2��Һ������2.24LCl2����״����ʱ����0.1mol����ת��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ݻ���ͬ�����ܱ�����A��B�У������¶�Ϊ150�棬ͬʱ��A�����м���a mol HI����B�����м���b mol HI ��a��b��������Ӧ2HI ��g��⇌H2��g��+I2��g�� �ﵽƽ�������˵����ȷ���ǣ���
A�� Ӧ��ʼ�ﵽƽ�⣬����ʱ��tA��tB
B�� ƽ��ʱ C��I2��A=C��I2��B
C�� ƽ��ʱI2�����ڻ�������е����������A��B
D�� A��B��HI��ƽ��ֽ�����ȣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ�ǹ��ڷ�ӦA2��g��+3B2��g��⇌2C��g����H��0��ƽ���ƶ�ͼ�Σ�Ӱ��ƽ���ƶ���ԭ���ǣ���
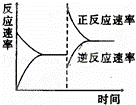
A�� �����¶ȣ�ͬʱ��ѹ
B�� �����¶ȣ�ͬʱ��ѹ
C�� ����Ӧ��Ũ�ȣ�ͬʱ��С������Ũ��
D�� ����Ӧ��Ũ�ȣ�ͬʱʹ�ô���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪������ˮ���ҷ�Ӧ��2Na+2H2O=2NaOH+H2��
��1����ͬ������Na��Mg��Al����������ᷴӦ������ͬ��״���£������û�����H2���������������
��2����ͬ���ʵ�����Na��Mg��Al����������ᷴӦ������ͬ״���£������û�����H2���������������
��3��Na��Mg��Al����������ᷴӦ������ͬ״���²����������������ȣ���Na��Mg��Al���ֽ��������ʵ���֮���ǣ�
��4����Na��Mg��Al��0.3mol�ֱ�Ͷ�뵽��0.1mol HCl�������У�ͬ��ͬѹ�²�����������������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com