
【题目】将①蔗糖、②淀粉、③纤维素、④蛋白质在稀硫酸作用下分别进行水解,最终水解产物只有1种的是( )
A.①②B.仅③C.④D.②③
科目:高中化学 来源: 题型:
【题目】某无色溶液中含有K+、Cl-、OH-、SO![]() 、SO
、SO![]() ,为检验溶液中所含的某些阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞溶液。检验其中OH-的实验方法省略,检验其他阴离子的过程如下图所示。
,为检验溶液中所含的某些阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞溶液。检验其中OH-的实验方法省略,检验其他阴离子的过程如下图所示。

(1)图中试剂①~⑤溶质的化学式分别是
①________,②________,③________,④__________,⑤__________。
(2)图中现象a、b、c表明检验出的离子分别是a________、b________、c________。
(3)白色沉淀A加试剂②反应的离子方程式_________________。
(4)无色溶液C加试剂③的主要目的是_____________________。
(5)白色沉淀A若加试剂③而不加试剂②,对实验的影响是____________________。
(6)气体E通入试剂④发生反应的离子方程式是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】超顺磁性的Fe3O4粒子(粒子平均直径为25nm)在医疗上有重要作用,实验室制备方法如下:在有N2保护和剧烈搅拌条件下,向FeCl3、FeCl2混合溶液中滴加氨水,可得到黑色的Fe3O4。实验装置如图:
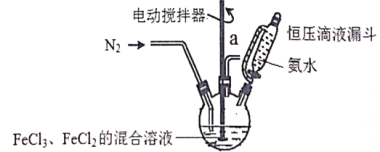
请回答下列问题:
(1)恒压滴液漏斗的优点是______________________。
(2)充N2的目的是___________,反应温度应控制在50℃,加热方法为___________。
(3)制备超顺磁性Fe3O4粒子反应原理的离子方程式为______________________。
(4)充分反应后,将三颈烧瓶中的混合物通过离心分离,然后水洗,最后用无水乙醇洗涤,用无水乙醇洗涤的优点是___________;为了验证得到的固体是超顺磁性的Fe3O4粒子,实验操作:_______________。为了检验超顺磁性粒子中含有+2价的铁,需要的化学试剂为___________(填代号)。
A.KSCN溶液 B.HCl溶液 C.H2O2溶液 D.K3[Fe(CN)6]溶液
(5)实验制得的超顺磁性的Fe3O4粒子中含有少量的Fe(OH)3,为测得Fe3O4的含量,称取mg试样,放在小烧杯中用足量稀硫酸溶解后定容于100mL容量瓶中,准确量取其中的20.00mL溶液置于锥形瓶中,然后用cmol/L的KMnO4溶液进行滴定,当______________________停止滴定,然后重复二次滴定,平均消耗KMnO4溶液ⅴmL,该样品的纯度为___________。(已知MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】摩尔质量是指单位物质的量的物质所含有的质量。
(1)已知NH3的相对分子质量为17,则NH3的摩尔质量为____。
(2)NA为阿伏加德罗常数,已知a g某气体中含分子数为b,则该气体的摩尔质量为 ____。
(3)已知一个铁原子的质量为b g,则铁的摩尔质量为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在25℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,则该反应的燃烧热的热化学方程式应为_________________。
(2)化学反应的焓变与反应物和生成物的键能有关。所谓键能就是:在101kPa、298 K时,断开1 mol气态AB为气态A、气态B时过程的焓变,用ΔH298(AB)表示;断开化学键时ΔH>0[如H2(g)=2H(g) ΔH= +436 kJ·mol-1],形成化学键时ΔH<0[如2H(g)=H2(g) ΔH= - 436 kJ·mol-1]。
已知:H2(g)+Cl2(g)=2HCl(g) ΔH= -185 kJ·mol-1 ΔH298(H2)=+ 436 kJ·mol-1 ,ΔH298(Cl2)= +247 kJ·mol-1则ΔH298(HCl)=__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关煤的说法正确的是( )
A.煤的干馏、气化和液化都是物理变化
B.煤中含有苯、甲苯、二甲苯等芳香烃
C.通过煤的干馏可获得苯、甲苯等芳香烃
D.水煤气是通过煤的干馏得到的气体燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热值是指一定条件下单位质量的物质完全燃烧所放出的热量。已知H2(g)、CO(g)和CH3OH(l)的热值分别为143 kJ· g-1、10 kJ·g-1和23 kJ·g-1。请回答下列问题:
(1)写出CO燃烧反应的热化学方程式为__________________________________________。
(2)表示甲醇燃烧热的热化学方程式为__________________________________________。
(3)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为__________________________。
(4)白磷与氧可发生如下反应:P4(g)+5O2(g)![]() P4O10(g)。已知断裂下列化学键需要吸收的能量分别为:P—P a kJ/mol、P—O b kJ/mol、P=O c kJ/mol、O=O d kJ/mol根据图示的分子结构和有关数据计算该反应的反应热_____________。
P4O10(g)。已知断裂下列化学键需要吸收的能量分别为:P—P a kJ/mol、P—O b kJ/mol、P=O c kJ/mol、O=O d kJ/mol根据图示的分子结构和有关数据计算该反应的反应热_____________。
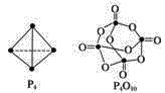
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,发生反应:①M(s)+N(g) R(g) ΔH= - Q1 kJ/mol
②2 R(g)+N(g) 2T(g) ΔH= - Q2 kJ/mol(已知Q1、Q2、Q3均为正值)
下列说法正确的是
A. 1molR(g)的能量总和大于1molM(s)与1molN(g)的能量总和
B. 将2mol R(g)与1molN(g)充分混合,在一定条件下充分反应,放出热量Q2 kJ
C. 当1molM(s)完全转化为T(g)时(假定无热量损失),放出热量(Q1+0.5Q2)kJ
D. M(g)+N(g) R(g) ΔH= - Q3 kJ/mol,则Q3 < Q1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,CO和CO2的混合气体共39.2 L,质量为61 g,则两种气体的物质的量之和为__________ mol,其中CO2为__________mol,CO占总体积的__________,混合气体的摩尔质量为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com