
A.C(s)+![]() O2(g)=CO(g);ΔH =-y kJ·mol-1??
O2(g)=CO(g);ΔH =-y kJ·mol-1??
B.2C(s)+2O2(g)=2CO(g);ΔH =-x kJ·mol-1??
C.C(s)+![]() O2(g)=CO(g);ΔH =-(2x-y) kJ·mo-1??
O2(g)=CO(g);ΔH =-(2x-y) kJ·mo-1??
D.2C(s)+O2(g)=2CO(g);ΔH =-(2x-y) kJ·mol-1??
 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源:新课程同步学案专家伴读 化学选修4(化学反应原理) 鲁科版 鲁科版 题型:013
|
在298 K、1.01×105 Pa下,12 g石墨在24 g氧气中燃烧至反应物完全消耗,测得放出x kJ的热量.已知在该条件下,1 mol石墨完全燃烧放出y kJ的热量.则右墨与氧气反应生成CO的热化学方程式表达正确的是 | |
| [ ] | |
A. |
C(石墨,s)+ |
B. |
C(石墨,s)+ |
C. |
C(石墨,s)+ |
D. |
2C(石墨,s)+O2(g)=2CO(g) ΔH=-(2x-y)kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年北京市顺义区高三尖子生综合素质展示化学试卷 题型:实验题
(10分)碘酸钾是一种白色结晶粉末,无臭无味。在酸性条件下碘酸钾是一种较强的氧化剂,与氢碘酸、二氧化硫等还原性物质作用,被还原为单质碘,在碱性介质中,碘酸钾能被氯气、次氯酸盐等氧化为高碘酸钾。碘酸钾在常温下稳定,加热至560 ℃开始分解。工业生产碘酸钾的流程如下图所示。
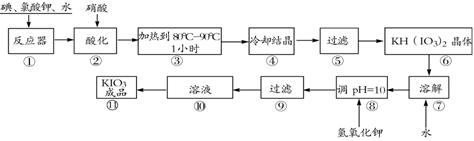
(1)在反应器中发生的反应I2+KClO3+H2O→KH(IO3)2+KCl+Cl2(未配平),生成两种还原产物所得电子数目相同,请写出已配平的该反应的化学方程式: 。
(2)步骤②中,用硝酸而不用HI,其原因可能是 。
(3)步骤③要保持溶液微沸1小时以完全排出氯气,排出氯气的原因为 。
(4)参照下表碘酸钾的溶解度,步骤⑾得到碘酸钾晶体,应采用的方法是 。
|
温度/℃ |
0 |
10 |
20 |
40 |
60 |
80 |
|
KIO3(g/100g水) |
4.60 |
6.27 |
8.08 |
12.6 |
18.3 |
24.8 |
(5)KIO3可用电解的方法制得,原理是以石墨为阳极,以不锈钢为阴极,在一定温度和电流下电解KI溶液。总反应方程式为KI+3H2O=KIO3+3H2↑,则阴极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在298K、1.01×105 Pa下,
A、C(石墨,s)+![]() O2(g)=CO(g) △H(298K)=-y kJ?mol―1
O2(g)=CO(g) △H(298K)=-y kJ?mol―1
B、C(石墨,s)+![]() O2(g)=CO(g) △H(298K)=-x kJ?mol―1
O2(g)=CO(g) △H(298K)=-x kJ?mol―1
C、C(石墨,s)+![]() O2(g)=CO(g) △H(298K)=-(2x-y)kJ?mol―1
O2(g)=CO(g) △H(298K)=-(2x-y)kJ?mol―1
D、2C(石墨,s)+O2(g)=2CO(g) △H(298K)=-(2x-y)kJ?mol―1
查看答案和解析>>
科目:高中化学 来源: 题型:
NA代表阿伏加德罗常数的值,下列说法正确的是
A.5.6 g 铁在足量氯气中燃烧,电子转移0.2 NA个
B.标准状况下,2.24 L水中含有0.1 NA个水分子
C.1.12 L氯气中含有0.1 NA个氯原子
D.12 g 石墨和金刚石的混合固体中,含碳原子 NA个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com