
X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。
这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。
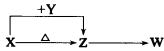
请回答:
(1)W的电子式是______________。
(2)X与Y在溶液中反应的离子方程式是___________________________。
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用下图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置Ⅴ中可收集到一种无色气体。

①装置Ⅰ中反应的化学方程式是______________________________。
装置Ⅱ中物质的化学式是_____________。
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置Ⅴ中气体,该化合物的化学式是__________,所需仪器装置是________(从上图选择必要装置,填写编号)。
(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是______________________________。
【答案】
(1)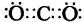
(2)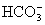 +OH-=
+OH-=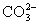 +H2O
+H2O
(3)①Na2CO3+H2SO4=Na2SO4+CO2↑+H2O
或2NaHCO3+H2SO4=Na2SO4+2CO2↑+2H2O
Na2O2
②H2O2
Ⅰ、Ⅳ、Ⅴ
(4)2Na2CO3+Cl2+H2O=NaClO+NaCl+2NaHCO3
【解析】由X、Y、Z的焰色反应均为黄色可知其中均含有Na元素,对照相互转化关系,确定X为NaHCO3、Y为NaOH、Z为Na2CO3、W为CO2。H、C、O、Na四种元素可能形成的气体有H2、CH4、O2、CO2等,结合各气体的性质可以确定装置V中收集到的是O2,各装置中药品及作用为:
| 编号 | 药品 | 作用 |
| I | Na2CO3或NaHCO3 | 产生CO2 |
| II | Na2O2 | 产生O2 |
| III | Ba(OH)2溶液 | 除去未反应的CO2 |
| IV | 浓硫酸 | 干燥O2气体 |
| V | —— | 收集O2 |


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
由熔盐电解法获得的粗铝含有一定量的金属钠和氢气,这些杂质可采用吹气精炼法除去,产生的尾气经处理后可用钢材镀铝。工艺流程如下:
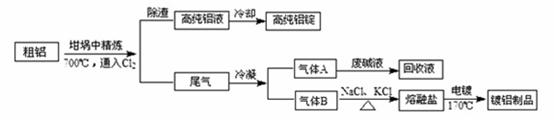
(注 :NaCl熔点为801℃;AlCl3在181℃升华)
:NaCl熔点为801℃;AlCl3在181℃升华)
(1)精炼前,需清除坩埚表面的氧化铁和石英砂,防止精炼时它们分别与铝发生置换反应产生新的杂质,相关的化学方程式为① 和② 。
(2)将Cl2连续通入坩埚中的粗铝熔体,杂质随气泡上浮除去。气泡的主要成分除Cl2外还含有 ;固态杂质粘附于气泡上,在熔体表面形成浮渣,浮渣中肯定存在 。
(3)在用废碱液处理A的过程中,所发生反应的离子方程式为 。
(4)镀铝电解池中,金属铝为 极,熔融盐电镀中铝元素和氯元素主要以AlCl4― 和Al2Cl7―形式存在,铝电镀的主要电极反应式为 。
(5)钢材镀铝后,表面形成的致密氧化铝膜能防止钢材腐蚀,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
钢铁工业对促进经济和社会发展起了重要作用。
(1)炼铁高炉分为五部分,铁矿石与高温煤气主要在_________部分发生反应,在______部分开始生成生铁和炉渣。
(2)炼钢时,除磷的化学方程式为_________;加入硅、锰和铝的目的是_______。
(3)不锈钢含有的Cr元素是在炼钢过程的氧吹_______(填“前”或“后”)加入,原因是_____________。
(4)炼铁和炼钢生产中,尾气均含有的主要污染物是_________。从环保和经济角度考虑,上述尾气经处理可用作________。
查看答案和解析>>
科目:高中化学 来源: 题型:
二氧化锰是制造锌锰干电池的基本材料。工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下:
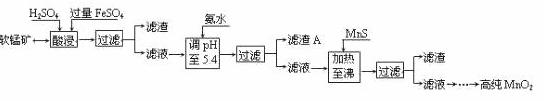
某软锰矿的主要成分为MnO2,还含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物。部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表,回答下列问题:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 | Zn(OH)2 | CuS | ZnS | MnS | FeS |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 | ≥–0.42 | ≥2.5 | ≥7 | ≥7 |
(1)硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的化学方程式为  。
。
(2)滤渣A的主要成分是 。
(3)加入MnS的目的是除去 杂质。
(4)碱性锌锰电池中,MnO2参与的电极反应方程式为 。
(5)从废旧碱性锌锰电池中可以回收利用的物质有 (写两种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下表中,对陈述I、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是
| 选项 | 陈述I | 陈述Ⅱ | 判断 |
| A | 工业生产硫酸用水吸收SO3 | SO3可与水反应 | I对;Ⅱ对;有 |
| B | Cl2和SO2混合后可用于漂白纸浆 | Cl2和SO2都有较好的漂白作用 | I对;Ⅱ错;无 |
| C | 金属钠具有强还原性 | 高压钠灯发出透雾性强的光 | I对;Ⅱ对;无 |
| D | 石墨常用作电解池的电极 | 石墨的化学性质稳定且导电性好 | I对;Ⅱ对;有 |
查看答案和解析>>
科目:高中化学 来源: 题型:
为配制0.1mol/L的NaOH溶液,下列说法中正确的是( )
|
| A. | 取4g NaOH固体溶于1L水中 |
|
| B. | 取0.4g NaOH固体溶于水配成1L溶液 |
|
| C. | 取4g NaOH固体溶于水配成1L溶液 |
|
| D. | 取0.4g NaOH固体溶于1L水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列化学方程式中,能够用离子方程式Ba2++SO42﹣=BaSO4↓表示的是( )
|
| A. | BaCl2+K2SO4=BaSO4↓+2KCl |
|
| B. | BaCO3+H2SO4=BaSO4↓+CO2↑+H2O |
|
| C. | Ba(OH)2+H2SO4=BaSO4↓+2H2O |
|
| D. | Ba(OH)2+2KHSO4=BaSO4↓+K2SO4+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期表是学习化学的重要工具,如图是元素周期表中的一格,下面从该图获取的信息中,正确的是( )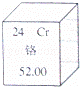
|
| A. | 该元素的原子序数为52 |
|
| B. | 该元素属于非金属元素 |
|
| C. | 该元素在地壳中的含量为52.00% |
|
| D. | 该元素的原子核外有24个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com