
 科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如下图所示)。已知该分子中N
科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如下图所示)。已知该分子中N -N-N键角都是108.1°,下列有关N(NO2) 3的说法正确的是
-N-N键角都是108.1°,下列有关N(NO2) 3的说法正确的是
A.分子中N、O间形成的共价键是非极性键
B.分子中四个氮原子共平面
C.该物质既有氧化性又有还原性
D.15.2g该物质含有6.02×1022个原子
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
200 mL 0.3 mol·L-1的K2SO4溶液和100 mL 0.2 mol·L-1的Fe2(SO4)3溶液混合后,若忽略液体混合时体积的变化,则溶液中SO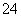 的物质的量浓度为
的物质的量浓度为
A.0.3 mol·L-1 B.0.4 mol·L-1 C.0.45 mol·L-1 D.0.5 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
[化学——选修3;物质结构与性质](15分)
周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。回答下列问题;
(1)b、c、d中第一电离能最大的是________(填元素符号),e的价层电子轨道示意图为________。
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为______;分子中既含有极性共价键、又含有非极性共价键的化合物是________(填化学式,写出两种)。
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是________;酸根呈三角锥结构的酸是________。(填化学式)
(4)e和c形成的一种离子化合物的晶体结构如图(a),则e离子的电荷为________。
(5)这5种元素形成的一种1∶1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构[如图(b)所示]。


(a) (b)
该化合物中,阴离子为________,阳离子中存在的化学键类型有________;该化合物加热时首先失去的组分是________,判断理由是______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
前四周期原子序数依次增大的元素A,B,C,D中,
A和B 的价电子层中未成对电子均只有1个,平且A-和B+
的价电子层中未成对电子均只有1个,平且A-和B+
 的电子相差为8;与B位于同一周期的C和D,它们价
的电子相差为8;与B位于同一周期的C和D,它们价
电子层中的未成对电子数分别为4和2,且原子序数
相差为2。
回答下列问题:
(1)D2+的价层电子排布图为_______。
(2)四种元素中第一电离最小的是________,
电负性最大的是________。(填元素符号)
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。
①该化合物的化学式为_________;D的配位数为_______;
②列式计算该晶体的密度_______g·cm-3。
(4)A-、B+和C3+三种离子组成的化合物B3CA6,其中化学键的类型有_____;该化合物中存在一个复杂离子,该离子的化学式为_______,配位体是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)元素的第一电离能:Al________Si(填“>”或“<”)。
(2)基态Mn2+的核外电子排布式为________。
(3)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是_________________________________。

(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如下图所示:

①在Xm-中,硼原子轨道的杂化类型有________;配位键存在于________原子之间(填原子的数字标号);
m=________(填数字)。
②硼砂晶体由Na+、Xm-和H2O构成,它们之间存在的作用力有________ (填序号)。
A.离子键 B.共价键 C.金属键
D.范德华力 E.氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
 是常规核裂变产物之一,可以通过测定大气或水中
是常规核裂变产物之一,可以通过测定大气或水中 的含量变化来检测核电站是否发生放射性物质泄漏。下列有关
的含量变化来检测核电站是否发生放射性物质泄漏。下列有关 的叙述中错误的是
的叙述中错误的是
A.  的化学性质与
的化学性质与 相同 B.
相同 B.  的原子序数为53
的原子序数为53
C.  的原子核外电子数为78 D.
的原子核外电子数为78 D.  的原子核内中子数多于质子数
的原子核内中子数多于质子数
查看答案和解析>>
科目:高中化学 来源: 题型:
用于金属焊接的某种焊条,其药皮由大理石、水泥、硅铁等配制而成。
(1)Al的原子结构示意图为_____________________;Al与NaOH溶液反应的离子方程式为
________________________________________________。
(2)30Si的原子的中子数为_________;SiO2晶体类型为__________________。
(3)Al3+与Yn-的电子数相同,Y所在族的各元素的氢化物的水溶液均显酸性,则该族氢化物中沸点最低的是________。
(4)焊接过程中,药皮在高温下产生了熔渣和使金属不被氧化的气体,该气体是__________。
(5)经处理后的熔渣36.0g(仅含Fe2O3、Al2O3、SiO2),加入足量稀盐酸,分离得到11.0g固体;滤液中加入过量NaOH溶液,分离得到21.4g固体;则此熔渣中Al2O3的质量分数为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.聚丙烯的结构简式为:
B.石英的化学式为:CaSiO3
C.在CS2、PCI3中各原子最外层均能达到8电子的稳定结构
D.Ar原子的结构示意图为:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com