
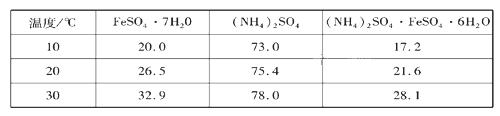
硫酸亚铁可与等物质的量的硫酸铵生成硫酸亚铁铵:(NH4)2SO4·FeSO4·6H2O,商品名称为莫尔盐,是一种复盐。一般亚铁盐在空气中易被氧气氧化,形成复盐后就比较稳定。与其他复盐一样,硫酸亚铁铵在水中的溶解度比组成它的每一种盐的溶解度都小,且几乎不溶于乙醇,利用这一性质可以制取硫酸亚铁铵晶体。三种盐的溶解度(单位为g/l00gH2O)见下表:
实验用品: Fe屑(含少量碳)、3mol/LH2SO4、( NH4)2SO4、蒸馏水、无水乙醇。
实验步骤流程图:
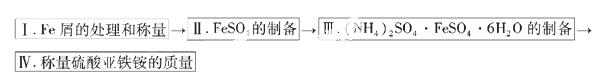
请完成以下实验记录:
(1)步骤I中用10% Na2CO3的热溶液处理铁屑的目的是 ,经处理后的干燥铁屑质量记为m1;
(2)将称量好的Fe屑放入锥形瓶中, 加入适量3mol/LH2SO4溶液,放在水浴中加热至气泡量产生较少时为止(有氢气生成,用明火加热注意安全)。趁热过滤,并用少量热水洗涤锥形瓶及滤纸,将滤液和洗涤液一起转移至蒸发皿中。将滤纸上的固体常温干燥后称重,记为m2;
加入适量3mol/LH2SO4溶液,放在水浴中加热至气泡量产生较少时为止(有氢气生成,用明火加热注意安全)。趁热过滤,并用少量热水洗涤锥形瓶及滤纸,将滤液和洗涤液一起转移至蒸发皿中。将滤纸上的固体常温干燥后称重,记为m2;
(3)称取一定质量的(NH4)2SO4,加入______ g(用含m1和m2的代数式表示,要求化简,下同。)水配制成室温下(20℃)的饱和溶液,并将其加入到上面实验的蒸发皿中,缓缓加热,浓缩至表面出现结晶薄膜为止。放置冷却,得到硫酸亚铁铵的晶体,过滤后用____________洗涤晶体。
(4)产品纯度的测定
先称取产品1.600g,加水溶解,配成100ml溶液,移取25.00mL待测溶液与锥形瓶中,再用硫酸酸化的0.0100mol/LKMnO4标准溶液进行滴定其中的Fe2+,达到滴定终点时消耗标准液的平均值为20.00mL,则样品中的(NH4)2SO4·FeSO4·6H2O的质量分数?(列式计算)
科目:高中化学 来源: 题型:
关于金属元素在自然界存在的情况的叙述中,正确的是( )
A.金属元素仅存在于矿物中
B.金属元素存在于矿物和动物体内,植物体内不含
C.少数金属元素以游离态存在,大多数金属元素以化合态存在
D.金属元素在自然界中都以化合态形式存在
查看答案和解析>>
科目:高中化学 来源: 题型:
把一块镁铝合金投入到1mol/L 盐酸里,待合金完全溶解后,往溶液里加、
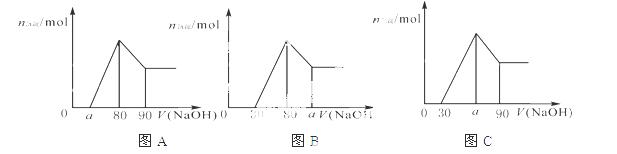
入1mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如下图A所示。下列说法中
不正确的是( )
 A.
A.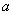 的取值范围为0≤ a<50
的取值范围为0≤ a<50
B.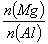 的最大值为2.5
的最大值为2.5
C.若将关系图改为B图时,则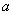 的取值范围为80<a<90
的取值范围为80<a<90
D.若将关系图改为C图时,则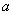 的取值范围为75<a<90
的取值范围为75<a<90
查看答案和解析>>
科目:高中化学 来源: 题型:
在FeCl3和CuCl2的混合溶液中加入铁屑,反应结束后滤出固体物质,滤液中的阳离子可能是 ( )
①只有Fe2+ ②Fe2+和Fe3+
③Fe2+和Cu2+ ④Cu2+和Fe3+
A.①③ B.②④ C.①④  D.②③
D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
中学化学常见物质甲、乙、丙、丁之间存在转化关系:甲十乙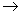 丙十丁。下列说法正确的是
丙十丁。下列说法正确的是
A.若甲为钠单质,丁为氢气,则乙一定是水
B.若甲为铝单质,丁为铁单质,则乙一定是氧化铁
C.若甲为铜单质,丁为氯化亚铁溶液,则乙一定是氯化铁溶液
D.若甲、乙、丙、丁均为化合物,则该反应一定属于复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
向5 mL NaCl溶液中滴入一滴AgNO3溶液,出现白色沉淀,继续滴加一滴KI溶液并振荡,沉淀变为黄色,再滴入一滴Na2S溶液并振荡,沉淀又变成黑色,根据上述变化过程,分析此三种沉淀物的溶解度关系为( )
A.AgCl=AgI=Ag2S B.AgCl<AgI<Ag2S
C.AgCl>AgI>Ag2S D.AgI>AgCl>Ag2S
查看答案和解析>>
科目:高中化学 来源: 题型:
已知难溶电解质在水溶液中存在溶解平衡:
MmAn(s)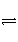
 mMn+(aq)+nAm-(aq)
mMn+(aq)+nAm-(aq)
Ksp=[Mn+]m·[Am-]n,称为溶度积。
某学习小组欲探究CaSO4沉淀转化为CaCO3沉淀的可能性,查得如下资料:(25℃)
| 难溶电 解质 | CaCO3 | CaSO4 | MgCO3 | Mg(OH)2 |
| Ksp | 2.8×10-9 mol-2·L-2 | 9.1×10-6 mol-2·L-2 | 6.8×10-6 mol-2·L-2 | 1.8×10-12 mol-3·L-3 |
实验步骤如下:
①往100 mL 0.1 mol·L-1的CaCl2溶液中加入100 mL 0.1 mol·L-1的Na2SO4溶液,立即有白色沉淀生成。
②向上述悬浊液中加入固体Na2CO3 3 g,搅拌,静置,沉淀后弃去上层清液。
③再加入蒸馏水搅拌,静置,沉淀后再弃去上层清液。
④________________________________________________________________________。
(1)由题中信息知Ksp越大,表示电解质的溶解度越______(填“大”或“小”)。
(2)写出第②步发生反应的化学方程式:
________________________________________________________________________
________________________________________________________________________。
(3)设计第③步的目的是
________________________________________________________________________。
(4)请补充第④步操作及发生的现象:
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
现向含6 mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示。
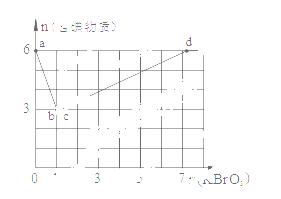
请回答下列问题:
(1)b点时,KI反应完全,则消耗的氧化剂与还原剂物质的量之比为 ▲ 。
(2)已知b→c过程中,仅有一种元素发生化合价变化,写出并配平该反应的离子方程式 _____________________▲___________________。
(3)n( KBrO3) = 4时,对应含碘物质的化学式为 ▲
KBrO3) = 4时,对应含碘物质的化学式为 ▲  。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com