
A、CH3CH=CH2发生加聚反应:nCH3CH=CH2
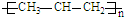 | ||||||
B、乙酸乙酯在酸性条件下水解:CH3COOCH2CH3+H2
| ||||||
| C、SO2通入到BaCl2溶液中:SO2+Ba2++H2O═BaSO3↓+2H+ | ||||||
| D、Fe(NO3)2溶液中滴加稀盐酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
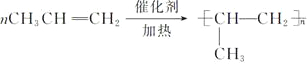 ,故A错误;
,故A错误;18 |
| 稀硫酸 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、SO2具有氧化性,可用于漂白纸浆 |
| B、炭具有还原性,一定条件下能将二氧化硅还原为硅 |
| C、BaCO3、BaSO4都难溶于水,均可用做钡餐 |
| D、Al2O3具有很高的熔点,可用于制造熔融烧碱的坩埚 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯、聚氯乙烯和苯分子均含有碳碳双键 |
| B、乙烷和丙烷互为同系物,蔗糖和麦芽糖互为同分异构体 |
| C、甲烷和氯气反应生成一氯甲烷,与苯和硝酸反应生成硝基苯的反应类型相同 |
| D、不同油脂水解都有甘油生成,不同的蛋白质水解都有氨基酸生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | … |
| CH4 | CH2O | CH2O2 | CH4O | C2H6 | C2H4O | C2H4O2 |
C2H6O |
| A、3种 | B、4种 | C、5种 | D、6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com