
【题目】已知A,B,C是中学化学常见物质,它们在一定条件下有如下转化关系 ![]()
(1)若A是一种淡黄色固体,B是造成酸雨的“罪魁祸首”.则X的化学式为 .
(2)若A一种黄绿色气体,X是生活中使用最广泛的一中金属.则B与金属Cu反应的离子方程式为 .
(3)若A是无色有刺激性气味的气体,B在空气中会立即转变为红棕色,则 A气体与X反应的化学方程式为 .
【答案】
(1)O2
(2)2Fe3++Cu=2Fe2++Cu2+
(3)4NH3+5O2  ?4NO+6H2O
?4NO+6H2O
【解析】解:(1)如A是淡黄色固体,B是造成酸雨的“罪魁祸首”,则A为S单质,X为O2 , B为SO2 , C为SO3 , 所以答案是:O2;(2)若A一种黄绿色气体,X是生活中使用最广泛的一中金属,则A为Cl2 , X为Fe,B为FeCl3 , C为FeCl2 ,
则B与金属Cu反应的离子方程式为:2Fe3++Cu=2Fe2++Cu2+ , 所以答案是:2Fe3++Cu=2Fe2++Cu2+;(3)若A是无色有刺激性气味的气体,B在空气中会立即转变为红棕色,则A为NH3 , X为O2 , B为NO,C为NO2 , A气体与X反应的化学方程式为:4NH3+5O2  4NO+6H2O,所以答案是:4NH3+5O2
4NO+6H2O,所以答案是:4NH3+5O2  4NO+6H2O.
4NO+6H2O.


科目:高中化学 来源: 题型:
【题目】下列关于醇化学性质的说法正确的是( )
A.乙醇分子中的氢原子均可被金属钠取代
B.乙醇在浓硫酸作催化剂时加热至 140 ℃可以制备乙烯
C.交警检查司机酒后驾车是利用了乙醇能被重铬酸钾氧化的性质
D.所有的醇都可以被氧化为醛或酮
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X为一种常见酸的浓溶液,能使蔗糖变黑.A与X反应的转化关系如图所示,其中反应条件及部分产物已略去,下列有关说法正确的是( ) 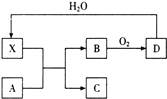
A.X能使蔗糖变黑主要体现了 X的强氧化性
B.若A为铁,则足量A与X在室温下即可完全反应
C.若A为碳单质,则将C通入少量澄清石灰水中,最终一定有白色沉淀产生
D.工业上,B转化为D的反应需使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子方程式CO32﹣+2H+═H2O+CO2↑中CO32﹣的代表的物质可以是( )
A.CaCO3
B.NaHCO3
C.Na2CO3
D.BaCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列两种物质混合后不能发生离子反应的是( )
A. 稀硝酸和碳酸钠溶液混合
B. 氯化钠溶液和硝酸银溶液混合
C. 硫酸钾溶液和氯化钡溶液混合
D. 硝酸钾溶液和氯化钡溶液混合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3是一种重要的化工原料,可用来制备肼、硝酸、硝酸铵和氯胺等。
(1)N2和H2以物质的量之比为1∶3在不同温度和压强下发生反应:N2+3H2![]() 2NH3,测得平衡体系中NH3的物质的量分数如右图。
2NH3,测得平衡体系中NH3的物质的量分数如右图。

① 下列途径可提高氨气产率的是________(填字母)。
a. 采用常温条件 b. 采用高温条件
c. 将原料气加压 d. 将氨液化,不断移去液氨
② 右图中所示的平衡体系中NH3的物质的量分数为0.549和0.478时,该反应的平衡常数分别为K1、K2,则K1________(填“>”“<”或“=”)K2。
(2)肼(N2H4)是一种火箭燃料。已知:
N2(g)+2O2(g)===2NO2(g);ΔH=+67.7 kJ·mol-1
N2H4(g)+O2(g)===N2(g)+2H2O(g);ΔH=-534.0 kJ·mol-1
NO2(g)===1/2N2O4(g);ΔH=-28.0 kJ·mol-1
① 反应2N2H4(g)+N2O4(g)===3N2(g)+4H2O(g)的ΔH=________kJ·mol-1。
② 氨气与次氯酸钠溶液反应生成肼的离子方程式为__________________________。
(3)电解硝酸工业的尾气NO可制备NH4NO3,其工作原理如右图。

① 阴极的电极反应式为____________________________________。
② 将电解生成的HNO3全部转化为NH4NO3,则通入的NH3与实际参加反应的NO的物质的量之比至少为________。
(4)饮用水消毒时,氯胺(NH2Cl等)在酸性条件下具有良好的效果(已知:NH2Cl+H2O≒NH3+HClO),其原因是__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将6. 0 mol L-1 H2SO4溶液由10 mL稀释至200 mL,再从中取出10 mL,这10 mL溶液中SO42-的物质的量浓度是
A. 0.05 mol L-1 B. 0.30 mol L-1
C. 0.15 mol L-1 D. 0.5 mol L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com