
| A. | 2:1 | B. | 3:1 | C. | 4:1 | D. | 5:1 |
分析 先根据方程式求出H2和C3H8的燃烧热,然后设出H2的物质的量,利用方程式组来解即可.
解答 解:设混合气中H2的物质的量为x,则C3H8的物质的量为5mol-x.根据题意,列方程为:285.8kJ/mol×x+2220.0kJ/mol×(5mol-x)=3847kJ,解得 x=3.75 mol;C3H8的物质的量为5mol-3.75mol=1.25mol.
所以混合气体中H2与C3H8的体积比即物质的量之比为3:1,故选B.
点评 以常规方法进行计算求解,思路直接,便于理解,为我们解题时的首选方法,但是由于一般需要列方程,步骤烦琐,计算量较大,可以选用十字交叉法,比较方便,但是理解起来有难度,根据个人情况进行相应计算即可.


科目:高中化学 来源: 题型:选择题
| A. | 10℃20mL 0.3mol•L-1的盐酸溶液 | B. | 20℃30mL 0.2mol•L-1的盐酸溶液 | ||
| C. | 20℃20mL 0.2 mol•L-1的盐酸溶液 | D. | 20℃30mL 0.4 mol•L-1的盐酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性:H2SO4>H3PO4 | B. | 碱性:NaOH>Mg(OH)2 | ||
| C. | 热稳定性:Na2CO3>NaHCO3 | D. | 非金属性:Cl>Br |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气使品红溶液褪色 | |
| B. | NO2 通入水中,气体由红棕色逐渐转变为无色 | |
| C. | 将铁片放入CuSO4溶液中,铁片表面有红色物质出现 | |
| D. | 向硅酸钠溶液中滴加适量的稀盐酸,有透明的凝胶形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
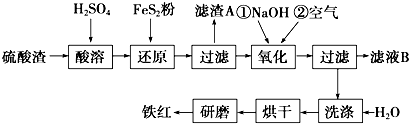
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com