


 ,故答案为:
,故答案为: ;
;| 10 |
| Vx |
| 20 |
| Vx |
| 5 |
| Vx |
| 10 |
| Vx |
| 5 |
| Vx |
| 5 |
| Vx |
| 10 |
| Vx |
| 5 |
| Vx |
| ||||
|
| ||
| 100 |
| ||
| 100 |


科目:高中化学 来源: 题型:
| 阳离子 | Fe3+、Ba2+、Al3+、Na+、Ag+ |
| 阴离子 | NO3-、OH-、SO42-、Cl-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小 |
| B、物质的溶解度随温度的升高而增加,故物质的溶解都是吸热的 |
| C、对于Al(OH)3(s)?Al(OH)3(aq)?Al3++3OH-,前者为溶解平衡,后者为电离平衡 |
| D、除溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3大 |
| E、沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
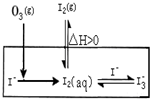 大气中的部分碘源于O3对海水中I-的氧化.将O3持续通入NaI酸性溶液溶液中进行模拟研究.
大气中的部分碘源于O3对海水中I-的氧化.将O3持续通入NaI酸性溶液溶液中进行模拟研究.
查看答案和解析>>
科目:高中化学 来源: 题型:
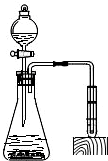 某校化学兴趣小组的同学用如图装置进行实验,已知分液漏斗、小试管中均盛有水.请回答下列问题:
某校化学兴趣小组的同学用如图装置进行实验,已知分液漏斗、小试管中均盛有水.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶度积就是溶解平衡时难溶电解质在溶液中的各离子浓度的乘积 |
| B、溶度积常数是不受任何条件影响的常数,简称溶度积 |
| C、可用离子积Qc判断沉淀溶解平衡进行的方向 |
| D、所有物质的溶度积都是随温度的升高而增大的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
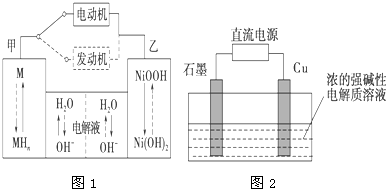 运用相关原理,回答下列问题:
运用相关原理,回答下列问题:| 1 |
| 2 |
| 3 |
| 2 |
| 放电 |
| 充电 |
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com