
���� ��1���ٵ�����ˮ�����ɰ����
�ڹ�֭�к�ά����C��������ΪӪ�����ʣ���ֱ�ӽ���ѪҺ������������ù��Ϊ���õĿ�����ҩ��ȿ���Ϊ��ɫ�����ֿ���Ϊ��������ʳ��ʳ�ù��������Ѫѹ���ߡ��������𣬰�˾ƥ���ǽ�����ʹҩ��
��� �⣺��1������������ĵ�������ø�Ĵ������£�����ˮ��Ϊ�����ᱻ�������գ��ʴ�Ϊ��B��
��ƻ��֭�к�ά����C��������ΪӪ�����ʣ���ֱ�ӽ���ѪҺ������������ù��Ϊ���õĿ�����ҩ��ȿ���Ϊ��ɫ�����ֿ���Ϊ��������ʳ��ʳ�ù��������Ѫѹ���ߡ��������𣬰�˾ƥ���ǽ�����ʹҩ���ʴ�Ϊ��C��D��E��B��A��
���� ����ע�⻯ѧ���������ϵ������֪ʶ��϶࣬�漰Ӫ���غ�ҩ�P��������ʵȻ���֪ʶ����Ŀ�ѶȲ���ע����ۻ�ѧ֪ʶ���ɽ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
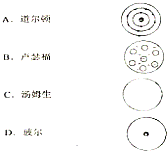 ��1�������п�ѧ�������ǵ�ԭ�ӽṹģ�ͣ���ͼ����������������
��1�������п�ѧ�������ǵ�ԭ�ӽṹģ�ͣ���ͼ�����������������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢ� | C�� | �ۢ� | D�� | �٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ñ���Na2CO3��Һ��ȥ����CO2�е�HCl���� | |
| B�� | ��Cl2��ȥFe2��SO4��3��Һ�е�����FeSO4 | |
| C�� | �ü��ȵķ�����ȥ����̼���ƹ����е�̼���������� | |
| D�� | ��AlCl3��Һ�м��������NaOH��Һ���Ʊ�Al��OH��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��H+��=10-13mol/L����Һ�У�NO3-��SO42-��K+��Na+ | |
| B�� | ��Fe3+����Һ���У�Na+��K+��CH3COO-��HCO3- | |
| C�� | �������ϡ���ᷴӦ�����Һ�У�[Al��OH��4]-��NH4+��Cl-��NO3- | |
| D�� | ������SO2��NO��N2��NH3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ʱ��Ӧʹ�������е�ˮ����ȫ���ɺ���ֹͣ���� | |
| B�� | ��Һ����ʱ����Һ©�����²�Һ����¿ڷų����ϲ�Һ����Ͽڵ��� | |
| C�� | ��ȥͭ���л��е�����þ�ۺ����ۿɼ�����������������Һ����Ӧ����ˡ�ϴ�� | |
| D�� | �������ᣬ�ų���ɫ���壬��������ʹ����ʯ��ˮ����ǵ����壬��ԭ��Һ����CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �л���A���������Ƿ��͵õ���Ҳ�ɴ���ţ������ȡ��������AΪ��ɫ��Һ�壬������ˮ��Ϊ�о�A�������ṹ������������ʵ�飺
�л���A���������Ƿ��͵õ���Ҳ�ɴ���ţ������ȡ��������AΪ��ɫ��Һ�壬������ˮ��Ϊ�о�A�������ṹ������������ʵ�飺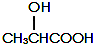 ��A��ŨH2SO4��ϣ���һ�������·�Ӧ������Ԫ��״��B��B�Ľṹ��ʽ
��A��ŨH2SO4��ϣ���һ�������·�Ӧ������Ԫ��״��B��B�Ľṹ��ʽ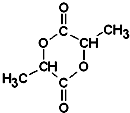 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.012 kg 12C�к���Լ6.02��1023��̼ԭ�� | |
| B�� | 1 mol H2O���2 mol���1 mol�� | |
| C�� | ���ʵ�������1 mol���ʵ����� | |
| D�� | 2 molˮ��Ħ��������1 molˮ��Ħ��������2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
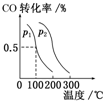 ���Ϲ�����仯�����2009��12��7��18���ڸ籾�����ٿ����й�������ŵ��2020�꣬��λGDP������̼�ŷű�2005���½�40%��45%��
���Ϲ�����仯�����2009��12��7��18���ڸ籾�����ٿ����й�������ŵ��2020�꣬��λGDP������̼�ŷű�2005���½�40%��45%���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com