
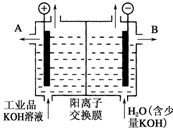
 氢氧化钾是重要的工业产品.请回答:
氢氧化钾是重要的工业产品.请回答:

 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 氧化 |
| 雨水 |
| 雨水 |
| 氧化 |
| A、若猜想一或猜想三正确,该雨水加入盐酸后,再加入BaCl2溶液,有白色沉淀生成 |
| B、若只存在猜想二的过程,则该雨水的pH随时间延长而增大 |
| C、若存在猜想二的过程,则该雨水可能使品红溶液褪色 |
| D、上述任意一个猜想正确,该地区雨水的pH均小于5.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
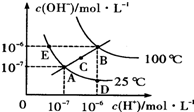
| A、图中五点KW间的关系B>C>A=D=E |
| B、若从A点到D点,可采用在水中加入少量酸的方法 |
| C、若从A点到C点,可用温度不变时在水中加入适量NH4Cl固体的方法 |
| D、若处在B点时,将pH=2的硫酸与pH=l2的KOH等体积混合后,溶液显碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol?L-1的氢氟酸溶液加水稀释,平衡正向移动,溶液中各离子浓度均减小 |
| B、pH=2的盐酸酸化的FeCl3溶液,稀释10倍后,溶液pH=3 |
| C、在NaHSO4溶液中,c(H+)=c(OH-)+c(SO42-) |
| D、在25℃时,任何水溶液中KW=1×10-14 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔是一种国际基本物理量 |
| B、通常状况下,气体摩尔体积约为22.4L |
| C、CO2的摩尔质量是44g |
| D、在同温同压下,相同体积的任何气体所含分子数相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com