
| A. | 只有①② | B. | 只有③④ | C. | 只有①②③ | D. | ①②③④ |
分析 ①发生反应:Fe+4HNO3=Fe(NO3)3+NO↑+2H2O;
②发生反应:3Fe3O4+28HNO3=9Fe(NO3)3+NO↑+14H2O;
③发生反应:3Fe(OH)2+10HNO3=3Fe(NO3)3+NO↑+8H2O;
④发生反应:3FeSO3+6HNO3=Fe(NO3)3+Fe2(SO4)3+3NO↑+3H2O,
根据方程式计算各物质消耗硝酸物质的量.
解答 解:①发生反应:Fe+4HNO3=Fe(NO3)3+NO↑+2H2O,3molFe消耗硝酸3mol×4=12mol,故①正确;
②发生反应:3Fe3O4+28HNO3=9Fe(NO3)3+NO↑+14H2O,3mol Fe3O4消耗28mol硝酸,故②正确;
③发生反应:3Fe(OH)2+10HNO3=3Fe(NO3)3+NO↑+8H2O,3molFe(OH)2消耗10molHNO3,故③正确;
④发生反应:3FeSO3+6HNO3=Fe(NO3)3+Fe2(SO4)3+3NO↑+3H2O,3 mol FeSO3消耗6mol HNO3,故④错误,
故选:C.
点评 本题考查化学方程式计算,明确发生的反应即可解答,侧重对化学方程式的考查.


科目:高中化学 来源: 题型:选择题
| A. | 铝片溶于过量的氢氧化钠溶液:Al+4OH-═AlO2-+2H2O | |
| B. | 0.01mol/LNH4Al(SO4)2溶液和0.02mol/LBa(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | |
| C. | 向Na2SiO3溶液中通入过量CO2:SiO32-+CO2+H2O═H2SiO3↓+CO32- | |
| D. | 向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2++2H2O═4Na++2Cu(OH)2↓+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S) | |
| B. | Na2C2O4溶液中:c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4)+c(C2O42-) | |
| C. | Na2CO3溶液:c(Na+)+c(H+)=2c(CO32-)+c(OH-) | |
| D. | CH3COONa和CaCl2混合溶液:c(Na+)+2c(Ca2+)=c(CH3COO-)+c(CH3COOH)+c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{2}{5}$mol | B. | $\frac{4}{5}$mol | C. | $\frac{6}{5}$mol | D. | $\frac{22}{5}$mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
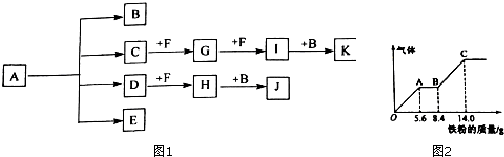
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 L 0.1mol•L-1的NaHCO3溶液中含有阳离子的物质的量为0.2mol | |
| B. | 0.1 mol水蒸气在标准状况下体积为2.24 L | |
| C. | 在25℃,1.01×105Pa时,11.2 L氧气所含的氧原子数目为6.02×1023 | |
| D. | 标准状况下,氧原子总数为0.2NA的SO2和O2的混合气体,其体积为2.24 L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com