
【题目】20 g A物质和14 g B物质恰好完全反应,生成8.8 g C物质、3.6 g D物质和0.2 mol E物质,则E物质的摩尔质量为( )
A. 100 g/mol B. 108 g/mol C. 55 g/mol D. 96 g/mol
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、R是元素周期表前四周期元素中的五种常见元素,其原子序数依次增大.X的基态原子的最外层电子排布式为nsnnpn+1 . Y、Z同主族且ZY2是导致酸雨的主要物质之一.R位于ds区且原子最外层只有一个电子.W原子次外层电子数为最外层电子数的7倍.请回答下列问题:
(1)W位于元素周期表第周期族,其基态原子的核外电子排布式为 .
(2)Y的气态氢化物的稳定性比Z的气态氢化物的稳定性(填“强”或“弱”).Y的第一电离能比Z的(填“大”或“小”).
(3)X的最常见的气态氢化物分子的VSEPR模型为 , 分子的空间构型是 .
(4)原子总数相同、价电子总数相同的分子或离子成为等电子体.分别写出一种与X02﹣互为等电子体的单质和化合物的化学式:、 . XO2﹣的中心原子采用杂化.
(5)[W(CN)6]3﹣离子中W的阳离子与CN﹣之间的共价键称为 , 该化学键能够形成的原因是 .
(6)图是R晶体的晶胞结构示意图,每个晶胞中含有个R原子. 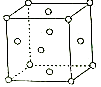
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应: N2 (g)+3H2(g)2NH3(g)
(1)若反应达平衡时某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,计算a的值;
(2)若反应达平衡时,混合气体的体积为716.8L(标况下),其中NH3的含量(体积分数)为25%.计算平衡时NH3的物质的量;
(3)原混合气体与平衡混合气体的总物质的量之比(最简整数比),n(始):n(平)= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器的名称、组装及使用方法是中学化学实验的基础,根据如图实验装置回答问题. 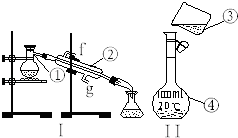
(1)写出下列仪器的名称:①;④;
(2)仪器①~④中,使用时必须检查是否漏水的是 . (填序号)
(3)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器有 , 将仪器补充完整后进行的实验操作的名称为;
(4)现需配制250mL、0.2mol/LNaCl溶液,装置II是某同学转移溶液的示意图,图中的错误之处: ①;② .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备1,2﹣二溴乙烷的反应原理如下:CH3CH2OH ![]() CH2=CH2 , CH2=CH2+Br2→BrCH2CH2Br.用少量的溴和足量的乙醇制备1,2﹣二溴乙烷的装置如右图所示,有关数据如表:
CH2=CH2 , CH2=CH2+Br2→BrCH2CH2Br.用少量的溴和足量的乙醇制备1,2﹣二溴乙烷的装置如右图所示,有关数据如表: 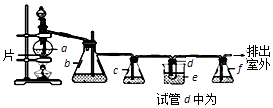
乙醇 | 1,2﹣二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/gcm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | ﹣130 | 9 | ﹣116 |
回答下列问题:
(1)在装置c中应加入(选填序号),其目的是吸收反应中可能生成的酸性气体. ①水 ②浓硫酸 ③氢氧化钠溶液 ④饱和碳酸氢钠溶液
(2)将二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在水的 层.(填“上”或“下”)
(3)判断d管中制备二溴乙烷反应已结束的最简单方法是 .
(4)若产物中有少量未反应的Br2 , 最好用(填正确选项前的序号)洗涤除去. ①水 ②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(5)以1,2﹣二溴乙烷为原料,制备聚氯乙烯,为了提高原料利用率,有同学设计了如下流程:1,2﹣二溴乙烷通过(①)反应制得(②),②通过(③)反应制得氯乙烯,由氯乙烯制得聚氯乙烯. ①(填反应类型),其化学方程式 .
②(填反应类型).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 分液时下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出
B. pH试纸使用时不需要润湿,红色石蕊试纸检测气体时也不需要润湿
C. 用药匙取用粉末状或小颗粒状固体
D. 蒸馏时蒸馏烧瓶中的液体尽量多些,加沸石进行蒸馏,但液体也不能蒸干
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在浓度均为3mol/L的盐酸和硫酸各100mL溶液中,分别加入等质量的铁粉,充分反应后生成气体质量之比为3:4.则加入铁粉的质量是( )
A.1.8 g
B.11.2 g
C.5.6 g
D.8.4 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重要有机物M和N常用于交联剂、涂料、杀虫剂等,合成路线如图所示: 
已知:
i ![]()
ii 
iii N的结构简式: ![]()
请回答下列问题:
(1)A中含氧官能团的名称为 , 由A生成B的反应类型为 .
(2)Z的名称为
(3)1molM在一定条件下发生加成反应,最多消耗molH2 .
(4)由B生成C的反应①的化学方程式为 .
(5)由Y生成D的化学方程式为 .
(6)G的同分异构体有多种,其中与G具有相同官能团的同分异构体有种,写出核磁共振氢谱有5组峰值,且峰值比为2:2:2:1:1的结构简式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com