
【题目】已知A(g)+B(g)![]() C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/℃ | 700 | 900 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应逆反应的△H_____0(填“<”“>”“=”)。
(2)830℃时,向一个5L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003mol·L-1·s-1。则6s时c(A)=_____________,C的物质的量为_____________;若反应经一段时间后,达到平衡时A的转化率为_______________,如果这时向该密闭容器中再充入1mol氩气,平衡时A的转化率为 ___________________。
(3)1200℃时反应C(g)+D(g)![]() A(g)+B(g)的平衡常数的值为____________。
A(g)+B(g)的平衡常数的值为____________。
【答案】 > 0.022mol·L-1 0.09mol 80% 80% 2.5
【解析】(1)由表中数据可知,温度越高平衡常数越小,说明升高温度平衡向逆反应移动,故正反应是放热反应,即△H<0;(2)反应初始6s内A的平均反应速率v(A)=0.003molL-1s-1,则6s内△c(A)=0.003molL-1s-1×6s=0.018mol/L,A的起始浓度为0.2mol÷5L=0.04mol/L,故6s时时c(A)=0.04mol/L-0.018mol/L=0.022mol/L,故6s内△n(A)=0.018mol/L×5L=0.09mol,由方程式可知n(C)=△n(A)=0.09mol;设平衡时A的浓度变化量为x,则:
A(g)+B(g)![]() C(g)+D(g)
C(g)+D(g)
起始浓度(mol/L):0.04 0.16 0 0
变化浓度(mol/L):x x x x
平衡浓度(mol/L):0.04-x 0.16-x x x
故x2/(0.04-x)(0.16-x)=1
解得x=0.032
所以平衡时A的转化率为![]() ×100%=80%
×100%=80%
体积不变,充入1mol氩气,反应混合物各组分的浓度不变,平衡不移动,A的转化率不变,仍然为80%;(3)同一反应在相同温度下,正、逆反应方向的平衡常数互为倒数,故1200℃时反应C(g)+D(g)![]() A(g)+B(g)的平衡常数的值为1÷0.4=2.5。
A(g)+B(g)的平衡常数的值为1÷0.4=2.5。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在酸性溶液中,下列各组离子能大量共存的是( )
A.K+、Fe3+、SO ![]() 、NO3﹣
、NO3﹣
B.Cu2+、Mg2+、SO ![]() 、Cl﹣
、Cl﹣
C.Ag+、Na+、NO3﹣、Cl﹣
D.K+、Na+、CO ![]() 、OH﹣
、OH﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏如皋落户。用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示。下列说法正确的是

A. 放电时,乙电极反应为:Ni(OH)2+OH- e=NiO(OH)+H2O
B. 放电时,甲电极为正极,OH移向乙电极
C. 电池总反应为H2+2NiO(OH) ![]() 2Ni(OH)2
2Ni(OH)2
D. 充电时,电池的碳电极与直流电源的正极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知2NO2(红棕色)![]() N2O4(无色)可以同时相互转化,①在密封有NO2的玻璃瓶中,升高温度,颜色加深,问NO2转化为N2O4是一个__________(填“吸热”或“放热”)反应;②在一个恒温恒压容器中,通入稀有气体。颜色_______(填“变深”、“变浅”或“不变”),平衡________移动(填“正向”、“逆向”或“不”下同);③在一个密闭恒容体系中,增大NO2的量,会引起NO2转化率________(填“增大”、“减小”或“不变”),颜色_______,再通入稀有气体增大压强,平衡________移动,颜色_________。
N2O4(无色)可以同时相互转化,①在密封有NO2的玻璃瓶中,升高温度,颜色加深,问NO2转化为N2O4是一个__________(填“吸热”或“放热”)反应;②在一个恒温恒压容器中,通入稀有气体。颜色_______(填“变深”、“变浅”或“不变”),平衡________移动(填“正向”、“逆向”或“不”下同);③在一个密闭恒容体系中,增大NO2的量,会引起NO2转化率________(填“增大”、“减小”或“不变”),颜色_______,再通入稀有气体增大压强,平衡________移动,颜色_________。
(2)用焦炭还原NO2的反应为:2NO2(g)+2C(s)![]() N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:

①A、B两点的浓度平衡常数关系:Kc(A)_______Kc(B) (填 “﹥”、“<”或“﹦”)。
②A、B、C三点中NO2的转化率最高的是_____(填“A”或“B”或“C”)点。
③计算C点时该反应的压强平衡常数Kp(C)=______(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究铁和硫反应产物中铁的化合价为+2价或+3价或既有+2也有+3价,某同学设计了如下图所示的实验过程:(已知硫会溶于热碱溶液)
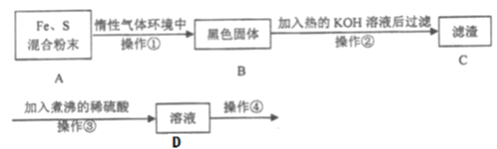
请回答以下问题:
(1)混合粉末A中S粉必须要过量,其原因是为了保证铁粉完全反应,从而避免_____。
(2)反应在“惰性气体环境中”进行的原因是______________________。
(3)操作①是用烧热的玻璃棒点触混合粉末,反应即可持续进行,这说明了_______。
(4)操作②的作用是________________________________________。
(5)操作③中稀硫酸煮沸的目的是____________________________________。
(6)为探究产物中铁的价态,需要继续对D溶液进行实验,请写出操作④的具体操作、现象及结论:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用平衡移动原理解释的是( )
A. 红棕色的NO2,加压后颜色先变深后变浅,但比原来要深
B. 高压比常压有利于SO2合成SO3的反应
C. 500 ℃时比室温更利于合成氨
D. 氯水在光照条件下颜色变浅,最终变为无色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用碳及其化合物的性质,完成下列小题:
(1)长期存放石灰水的瓶子内会出现一层白色固体,请分析这层白色固体产生的原因(用化学方程式表示);用完石灰水后,怎样除去瓶壁上的白色固体,(用化学方程式表示).
(2)除去碳酸钠固体中少量碳酸氢钠的方法是(用化学方程式表示):
(3)向碳酸氢钠溶液滴加NaOH溶液,发生反应的离子方程式为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气、甲醇是优质的清洁燃料,可制作燃料电池。
(1)已知:①CH3OH(l)+O2(g )= CO(g)+2H2O(g) △H= - 354.8 kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) △H= -566.0 kJ·mol-1
③H2O(g) = H2O(l) △H= -44.0 kJ·mol-1
请写出甲醇完全燃烧生成二氧化碳和液态水的热化学方程式:______________________________。
(2)某实验小组利用H2(g)、O2(g)、KOH(aq)设计成电池装置(装置Ⅰ),通过装置Ⅱ实现铁棒上镀铜。
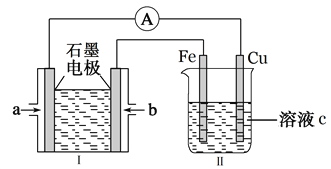
①装置Ⅰ中,a口通入的气体为____________(填“H2”或“O2”),放电时,溶液中的K+向______极移动(填“正”或“负”),该电池负极的电极反应式为______________________。
②装置Ⅱ中,溶液c可选用________________溶液。
若电镀结束后,装置Ⅱ中Fe电极的质量改变了12.8g,则装置Ⅰ中理论上消耗氧气的体积为________L(标准状况下)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com