
 H2(g)+I2(g)已达到平衡状态的是( )
H2(g)+I2(g)已达到平衡状态的是( ) H2+I2(g)的气体的计量数前后不变。(1)虽然表示的是不同的反应方向,但不能证明υ(正)=υ(逆),故不正确;(2)能表示υ(正)=υ(逆),则此项正确;(3)、(5)是浓度相等或成比例,并不能说明“定”的真正含义,故不正确;(4)速率之比虽然正确,但未指明正逆速率的关系,故不正确;(6)条件一定,某一生成物浓度不再变化,说明了“定”的真正含义,故正确;(7)对于反应2HI(g)
H2+I2(g)的气体的计量数前后不变。(1)虽然表示的是不同的反应方向,但不能证明υ(正)=υ(逆),故不正确;(2)能表示υ(正)=υ(逆),则此项正确;(3)、(5)是浓度相等或成比例,并不能说明“定”的真正含义,故不正确;(4)速率之比虽然正确,但未指明正逆速率的关系,故不正确;(6)条件一定,某一生成物浓度不再变化,说明了“定”的真正含义,故正确;(7)对于反应2HI(g) H2(g)+I2(g),前后气体体积不变,当温度、体积一定时,压强不变不能说明反应已达平衡状态;而对于反应2NO2
H2(g)+I2(g),前后气体体积不变,当温度、体积一定时,压强不变不能说明反应已达平衡状态;而对于反应2NO2 N2O4;前后气体体积不相等,当温度、体积一定时,压强不变能说明任何物质的物质的量不变,为“定”值,故反应已达平衡状态;(8)对于反应2HI(g)
N2O4;前后气体体积不相等,当温度、体积一定时,压强不变能说明任何物质的物质的量不变,为“定”值,故反应已达平衡状态;(8)对于反应2HI(g) H2(g)+I2(g),前后气体物质的量不变,质量不变,混合气体的平均相对分子质量不再变化不能说明反应已达平衡;而对于反应2NO2
H2(g)+I2(g),前后气体物质的量不变,质量不变,混合气体的平均相对分子质量不再变化不能说明反应已达平衡;而对于反应2NO2 N2O4,前后气体物质的量不相等,质量不变,混合气体的平均相对分子质量不再变化能说明任何物质的物质的量不变,为“定”值,故反应已达平衡;(9)混合气体的颜色不再发生变化,说明各物质的浓度不变,证明反应已达平衡状态;(10)对于反应2HI(g)
N2O4,前后气体物质的量不相等,质量不变,混合气体的平均相对分子质量不再变化能说明任何物质的物质的量不变,为“定”值,故反应已达平衡;(9)混合气体的颜色不再发生变化,说明各物质的浓度不变,证明反应已达平衡状态;(10)对于反应2HI(g) H2(g)+I2(g);前后气体物质的量不变,当温度、压强一定时,体积不变,密度不变,不能说明反应已达平衡状态;而对于反应2NO2
H2(g)+I2(g);前后气体物质的量不变,当温度、压强一定时,体积不变,密度不变,不能说明反应已达平衡状态;而对于反应2NO2 N2O4,前后气体物质的量不相等,当温度、压强一定时,体积不变,密度不变,能说明反应已达平衡状态。
N2O4,前后气体物质的量不相等,当温度、压强一定时,体积不变,密度不变,能说明反应已达平衡状态。

科目:高中化学 来源:不详 题型:填空题
 (3)你认为B、C、D元素形成的化合物之间_________(填“能”或“不能”)发生下面的反应BC+BD3 D BC2+D2C,得出上面结论的理由是________________。
(3)你认为B、C、D元素形成的化合物之间_________(填“能”或“不能”)发生下面的反应BC+BD3 D BC2+D2C,得出上面结论的理由是________________。 (4)Ⅰ.恒温恒压下,在一体积可变的密闭容器中发生下列反应:
(4)Ⅰ.恒温恒压下,在一体积可变的密闭容器中发生下列反应:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2SO3达到平衡后,再向反应容器中充入含氧的同位素
2SO3达到平衡后,再向反应容器中充入含氧的同位素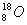 的氧气,经过一段时间后,
的氧气,经过一段时间后,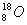 原子存在于( )
原子存在于( ) | A.O2 | B.SO2 |
| C.O2和SO2 | D.O2、SO2和SO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 C(g)3D(g);
C(g)3D(g);


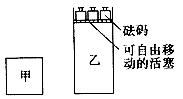

A.甲、乙两容器中的反应达到化学平衡时,两容器内压强相等 |
B.甲、乙两容器中的反应达到化学平衡时,C的体积分数相等 |
C.向甲容器中再充人2 molA和2 molB,平衡后甲中物质C的浓度不变 |
D.向乙容器中再充入2 molC和6 molD,平衡后乙中物质C的浓度为原来的2倍 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 xC(g),达到化学平衡后,C的体积分数为
xC(g),达到化学平衡后,C的体积分数为 。假设该反应的条件分别和下列各选项的条件相同,下列判断正确的是
。假设该反应的条件分别和下列各选项的条件相同,下列判断正确的是  时,按1.5 mol A、l mol C作为起始物质,达到平衡后, C的体积分数仍为
时,按1.5 mol A、l mol C作为起始物质,达到平衡后, C的体积分数仍为
 2时,将2mol C作起始物质,达到平衡后,C的体积分数仍为
2时,将2mol C作起始物质,达到平衡后,C的体积分数仍为
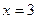 时,l mol A、1mol B、6mol C作起始物质,达到平衡后,C的体积分数仍为
时,l mol A、1mol B、6mol C作起始物质,达到平衡后,C的体积分数仍为
 ,则
,则 为2或3
为2或3查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
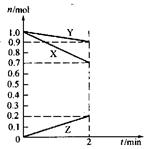
| A.反应过程中,若增大压强能提高SiCl4的转化率 |
| B.若反应开始时SiCl4为1mol,则达到平衡时,吸收热量为QkJ |
| C.反应至4min时,若HCl的浓度为0.12mol·L-1,则H2的反应速率为0.03mol/(L·min) |
| D.当反应吸收热量为0.025QkJ时,生成的HCl通入100mL1mol·L-1的NaOH恰好反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 催化剂 |
| △ |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.C的生成速率与C的分解速率相等 |
| B.混合气体的总物质的量不再变化 |
| C.A、B、C的浓度不再变化 |
| D.单位时间内生成amolA,同时生成3amolB |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com