
【题目】将E和F加入密闭容器中,在一定条件下发生反应:![]() 。忽略固体体积,平衡时G的体积分数
。忽略固体体积,平衡时G的体积分数![]() 随温度和压强的变化如下表所示:
随温度和压强的变化如下表所示:
1.0 | 2.0 | 3.0 | |
810 | 54.0 | a | b |
915 | c | 75.0 | d |
1000 | f | 83.0 |
下列判断不正确的是( )
A.该反应的![]()
B.K(1000℃)>K(810℃)
C.![]()
D.915℃,2.0MPa时E的转化率为![]()
科目:高中化学 来源: 题型:
【题目】将4molA和2molB放入2L密闭容器中发生反应2A(g)+B(g)![]() 2C(g) △H<0
2C(g) △H<0
,4s后反应达到平衡状态,此时测得C的浓度为0.6mol/L.下列说法正确的是( )
A.若不断增加A的质量,可使反应放出热量的数值达到2︱ΔH︱
B.4 s内,υ(B)=0.075 mol/(L ·s)
C.达到平衡状态后,若只升高温度,则C的物质的量浓度增大
D.达到平衡状态后,若温度不变,缩小容器的体积,则A的转化率降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
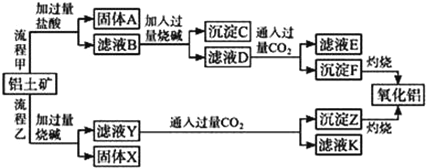
请回答下列问题:
(1)固体A的主要成分是______________(写名称).
(2)铝土矿与过量烧碱反应的离子方程式为______、______.
(3)电解熔融氧化铝可制得两种单质,写出该反应化学方程式______________.
(4)指出流程乙的一个缺点是____________.
(5)氧化铝与焦炭的混合物在氮气中高温加热反应,制得新型非金属材料AlN与一种中学常见气体X.已知每转移6.02×1023个电子,有0.5mol化合物X生成,此反应的化学方程式________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物。某同学依据溴乙烷的性质,验证取代反应时,反应需用水浴加热的原因是_____;观察到________现象时,表明溴乙烷与NaOH溶液已完全反应。
(2)有机物A的分子式为C3H8O,它能氧化成B也能与浓硫酸共热生成C。若B不能发生银镜反应,C不能使溴水褪色。B含有的官能团名称为__________,C结构简式为:_____________。
(3)DAP是电器和仪表部件中常用的一种高分子材料,其结构如图:
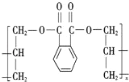
则合成它的单体是________(填序号)。
①邻苯二甲酸 ②丙烯 ③丙烯酸 ④邻苯二甲醇 ⑤丙烯醇
(4)![]() 的名称是(用系统命名法命名)_____________________。
的名称是(用系统命名法命名)_____________________。
(5)写出![]() 与足量溴水反应的化学方程式________。
与足量溴水反应的化学方程式________。
(6)写出 与足量NaOH溶液反应的化学方程式_____。
与足量NaOH溶液反应的化学方程式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的氨基甲酸置于恒容的密闭真空容器中(固体体积忽略不计),使其达到化学平衡:H2NCOONH4(s)![]() 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
平衡气体总浓度/10-3mol/L | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
下列有关叙述正确的是
A. 在低温下该反应能自发进行
B. 15℃时,该反应的化学平衡常数约为2.0
C. 当混合气体平均相对分子质量不变时,该反应达到化学反应限度
D. 恒温条件下,向原平衡体系中再充入2molNH3和1molCO2,达平衡后CO2浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用环己醇脱水的方法合成环己烯,该实验的装置如下图所示:

可能用到的有关数据如下:
相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 | |
环已醇 | 100 | 0.9618 | 161 | 微溶于水 |
环已烯 | 82 | 0.8102 | 83 | 难溶于水 |
按下列实验步骤回答问题:
Ⅰ.产物合成
在a中加入10.0g环己醇和2片碎瓷片,冷却搅拌下慢慢加入1mL浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度接近90℃。
(l)碎瓷片的作用是________;b的名称是________;
(2)a中发生主要反应的化学方程式为____________________________;本实验最容易产生的有机副产物的结构简式为________。
Ⅱ.分离提纯
将反应粗产物倒入分液漏斗中,依次用少量5%碳酸钠溶液和水洗涤,分离后加人无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过操作X得到纯净的环己烯,称量,其质量为4.1g。
(3)用碳酸钠溶液洗涤的作用是________,操作X的名称为________。
Ⅲ.产物分析及产率计算
(4)①核磁共振氢谱可以帮助鉴定产物是否为环己烯,环己烯分子中有_______种不同化学环境的氢原子。
② 本实验所得环己烯的产率是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L恒容密闭容器中投入![]() 和
和![]() ,分别在温度
,分别在温度![]() 和
和![]() 下进行如下反应:
下进行如下反应:![]() ,且在
,且在![]() 温度下反应一段时间后改变某一个外界条件,测得
温度下反应一段时间后改变某一个外界条件,测得![]() 的物质的量
的物质的量![]() 与时间
与时间![]() 关系如下表所示,下列有关说法中错误的是( )
关系如下表所示,下列有关说法中错误的是( )
0 | 5min | 10min | 15min | 20min | 25min | |
| 2mol |
|
|
|
|
|
| 2mol |
|
|
|
|
|
A.![]()
B.![]()
C.![]() 温度下15min时改变的条件可能是加入一定量的He
温度下15min时改变的条件可能是加入一定量的He
D.![]() 温度下的平衡常数为12.96
温度下的平衡常数为12.96
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向2l恒温恒容容器中加入2molMgSO4并充入 2molCO,发生反应:MgSO4(s)+ CO(g)![]() MgO(s)+ CO2(g)+SO2(g)△H > 0 。测得反应过程中残留固体的质量随时间变化如图所示,下列说法不正确的是
MgO(s)+ CO2(g)+SO2(g)△H > 0 。测得反应过程中残留固体的质量随时间变化如图所示,下列说法不正确的是
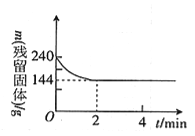
A. 0 ~2min内平均反应速率v(SO2)= 0.3 mol·l-1 ·min-1
B. 2 ~4min内容器内气体的密度没有变化
C. 该温度下,反应的平衡常数为1.8
D. 保持其他条件不变,起始时向容器中充入1.00 mol MgSO4和1.00 molCO,反应达到平衡时,n(CO2)> 0.60 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化铝(Al2O3) 和氮化硅(Si3N4)是优良的高温结构陶瓷,在工业生产和科技领域有重要用途。
(1)Al与NaOH溶液反应的离子方程式为_____________________________________。
(2)下列实验能比较镁和铝的金属性强弱的是____________(填序号)。
a.测定镁和铝的导电性强弱
b.测定等物质的量浓度的Al2(SO4)3和MgSO4溶液的pH
c.向0.1 mol/L AlCl3和0.1 mol/L MgCl2中加过量NaOH溶液
(3)铝热法是常用的金属冶炼方法之一。
已知:4Al (s)+3O2(g) =2Al2O3(s) ΔH1 = -3352 kJ/mol
Mn(s)+ O2(g) =MnO2 (s) ΔH2 = -521 kJ/mol
Al与MnO2反应冶炼金属Mn的热化学方程式是_____________________________。
(4)工业上用化学气相沉积法制备氮化硅,其反应如下:
3SiCl4(g) + 2N2(g) + 6H2(g) ![]() Si3N4(s) + 12HCl(g) △H<0
Si3N4(s) + 12HCl(g) △H<0
某温度和压强条件下,分别将0.3mol SiCl4(g)、0.2mol N2(g)、0.6mol H2(g)充入2L密闭容器内,进行上述反应,5min达到平衡状态,所得Si3N4(s)的质量是5.60g。
①H2的平均反应速率是_________ mol/(L·min)。
②若按n(SiCl4) : n(N2) : n(H2) = 3 : 2 : 6的投料配比,向上述容器不断扩大加料,SiCl4(g)的转化率应______(填“增大”、“减小”或“不变”)。
(5)298K时,Ksp[Ce(OH)4]=1×10—29。Ce(OH)4的溶度积表达式为Ksp=_______________。
为了使溶液中Ce4+沉淀完全,即残留在溶液中的c(Ce4+)小于1×10-5mol·L-1,需调节pH为______以上。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com