
分析 (1)依据C=$\frac{1000ρω}{M}$计算浓硫酸的物质的量浓度,依据溶液稀释前后溶质的物质的量不变计算需要浓硫酸体积;
(2)依据配制步骤选择合适的仪器;
(3)依据配制一定物质的量浓度溶液的一般步骤排序;
(4)分析不当操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析;
解答 解:(1)98%密度为1.84g/mL的浓硫酸物质的量浓度=$\frac{1000×1.84×98%}{98}$=18.4mol/L,设需要浓硫酸体积为V,依据溶液稀释前后溶质的物质的量不变,V×18.4mol/L=250mL×2mol/L,解得V=27.2mL;
故答案为:27.2;
(2)配制250ml 2mol/L的稀硫酸步骤为:计算、量取、稀释、移液、洗涤移液、定容、摇匀等操作,需要的仪器有:量筒、玻璃棒、胶头滴管、烧杯、250mL容量瓶,
故答案为:B、C、E、F、H;
(3)配制一定物质的量浓度溶液的一般步骤:计算、量取(称量)、稀释(溶解)、冷却、移液、洗涤、定容、摇匀、装瓶;
所以正确的顺序为:D、C、A、E、B、F、H、G;
故答案为:D、C、A、E、B、F、H、G;
(4)用量筒量取浓硫酸时,仰视量筒进行读数,导致量取的硫酸的物质的量偏高,溶液浓度偏高;
定容时,仰视观察容量瓶刻度线,导致溶液体积偏大,溶液浓度偏低;
故答案为:偏高 偏低.
点评 本题考查了配制一定物质的量浓度溶液,明确配制原理和步骤是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题

| A. | 实验①试管最终会充满水 | |
| B. | 实验②试管中溶液变为血红色 | |
| C. | 可用实验③装置除去CO2气体中含有的少量HCl杂质 | |
| D. | 实验④可观察丁达尔现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1级 | B. | 2级 | C. | 3级 | D. | 0级 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径按X、Y、Z、R、W的顺序依次增大 | |
| B. | 熔沸点:X2R>X2Y | |
| C. | Z与Y形成的化合物可作为耐高温材料 | |
| D. | WY2能与碱反应,但不能与任何酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
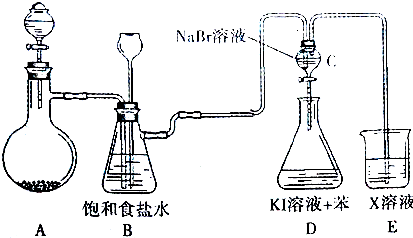
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com