
下列各组离子在指定溶液中,一定能大量共存的是
①c(H+)=10-12 mol·L-1的溶液中:I-、NO3-、SO32-、K+
②中性溶液中:Fe3+、NO3-、Na+、SO42-
③由水电离出的c(H+)=10-12mol/L的溶液:Ba2+、Na+、NO3-、Cl-
④使甲基橙变黄色的溶液中:CO32-、Na+ 、AlO2-、SO42-
A.①③ B.①④ C.②③ D.③④
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源:2014-2015河南省高二上学期第三次月考化学试卷(解析版) 题型:推断题
(10分)由短周期元素组成的A、B两种盐可发生下列变化,且B的焰色反应呈黄色(其它生成物未在图中列出)
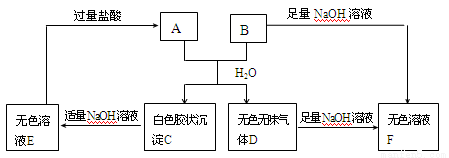
(1)无色溶液F中,一定含有的溶质的化学式为 。
(2)写出白色胶状沉淀C转化为无色溶液E的离子方程式________________。
(3)A和B的混合物溶于水发生反应的离子方程式______________________。
(4)将B与E的溶液混合时,可观察到的现象是_________________________,写出其反应的离子方程式__________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高一上学期第三次考试化学试卷(解析版) 题型:选择题
“纳米材料”是粒子直径为1~100nm的材料,纳米碳就是其中的一种,若将纳米碳均匀地分散到蒸馏水中,所形成的物质
①.是溶液 ②.是胶体 ③.能产生丁达尔效应 ④.能透过滤纸
⑤.不能透过滤纸 ⑥.静置后,会析出黑色沉淀
A.①④⑥ B.②③④ C.②③⑤ D.①③④⑥
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高二上学期第三次考试化学试卷(解析版) 题型:选择题
在下列装置中,MSO4和NSO4是两种常见金属的易溶盐。当K闭合时,SO42-从右到左通过交换膜移向M极,下列分析正确的是

A.溶液中c(M2+)减小
B.N的电极反应式:N===N2++2e-
C.X电极上有H2产生,发生还原反应
D.反应过程中Y电极周围生成白色胶状沉淀
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高二上学期第三次考试化学试卷(解析版) 题型:选择题
下列溶液中有关物质的量浓度关系不正确的
A.pH=2的HA溶液与pH=12的MOH溶液以任意比混合:c(H+)+c(M+)=c(OH-)+c(A-)
B.pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(CH3COONa)<c(Na2CO3)
C.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH)
D.0.1 mol·L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(A2-)>c(H2A)
查看答案和解析>>
科目:高中化学 来源:2014-2015甘肃省天水市高一上学期月考化学试卷(解析版) 题型:计算题
(14分)将镁、铝的混合物共0.2 mol, 溶于200 mL 4 mol·L—1的盐酸溶液中,然后再滴加2mol·L—1的NaOH溶液。请回答下列问题:

(1)若在滴加NaOH溶液的过程中,沉淀质量m 随加入NaOH溶液的体积V变化情况如图所示。当V1=160 mL时,则金属粉末中n (Al)= mol;
(2)0~V1段发生的反应的离子方程式为 ;
(3)若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+ 刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)= mL;
(4)若镁、铝的混合物仍为0.2 mol,其中镁粉的物质的量分数为a,改用200 mL 4mol·L—1的硫酸溶解此混合物后,再加入840mL 2 mol·L—1的NaOH溶液,所得沉淀中无Al(OH)3,则a的取值范围为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015甘肃省天水市高一上学期月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.金属在反应中只能作还原剂,非金属在反应中只能作氧化剂
B.氧化剂在反应中失去电子,还原剂在反应中得到电子
C.氧化剂具有氧化性,还原剂具有还原性
D.阳离子只有氧化性,阴离子只有还原性
查看答案和解析>>
科目:高中化学 来源:2014-2015甘肃省天水市高二上学期月考化学试卷(解析版) 题型:填空题
(共6分)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+ 2N2(g) 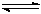 Si3N4(s) + 6CO(g)
Si3N4(s) + 6CO(g)
(1)该反应的氧化剂是 ,2molN2参加反应转移电子数为 。
(2)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率v与时间t的关系如图。
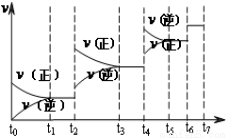
图中t4时引起平衡移动的条件可能是 ;图中表示平衡混合物中CO的含量最高的一段时间是 。
(3)若该反应的平衡常数为 K=729,则在同温度下1L密闭容器中,足量的SiO2和C与2mol N2充分反应,则N2的转化率是
(提示:272 = 729)
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省高二上学期1月质量检测化学试卷(解析版) 题型:选择题
下列说法正确的是
A.在一定温度下的AgCl水溶液中,Ag+和Cl-浓度的乘积是一个常数
B.AgCl的Ksp=1.8×10-10 mol2·L-2,在任何含AgCl固体的溶液中,[Ag+]=[Cl-],且Ag+和Cl-浓度的乘积等于1.8×10-10mol2·L-2
C.温度一定时,在AgCl饱和溶液中,Ag+和Cl-浓度的乘积是一个常数
D.向饱和AgCl溶液中加入盐酸,Ksp变大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com