
 .
.分析 (1)CH3+中C、H原子之间以共用电子对形成共价键,根据CH3+离子的价层电子对数判断杂化轨道类型金和空间构型;
(2)根据价层电子对互斥理论确定中心原子杂化方式及粒子的空间构型,价层电子对个数=σ键个数+孤电子对个数,σ键个数=配原子个数,孤电子对个数=$\frac{1}{2}$(a-xb),a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数.
解答 解:(1)CH3+离子的价层电子对数=3+$\frac{4-1-1×3}{2}$=3,应为sp2杂化,孤对电子对数为0,故为平面三角形,键角120°,因碳原子最外层4个电子,则CH3+是缺电子的碳正离子,可看作是甲基失去一个电子后的产物,甲基的电子式为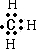 ,则CH3+的电子式为
,则CH3+的电子式为 ,
,
故答案为:sp2;平面三角形;120°; ;
;
(2)BeCl2分子中含孤电子对为$\frac{1}{2}$(2-2×1)=0,价层电子对个数是2,故为直线形结构;
SO42-中含孤电子对为$\frac{6+2-2×4}{2}$=0,价层电子对个数都是4,所以空间构型都是正四面体结构;
SO32-中孤对电子为$\frac{6+2-3×2}{2}$=1,σ 键电子对均为3,空间构型为三角锥形;
故答案为:直线形;正四面体形;三角锥形.
点评 本本题考查了电子式书写、杂化轨道类型的判断和分子离子空间构型的分析,注意判断中心原子的价层电子对以及孤对电子数的判断,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| X | |||
| Y | Z | W | A |
| T | B |
| A. | X、W、Z元素的原子半径与它们的气态氢化物的热稳定性变化趋势相反 | |
| B. | Y、Z、W、A元素性质均较为活泼,但其中Y、W在自然界中存在游离态的形式,它们的最高价氧化物的水化物的酸性依次递增 | |
| C. | 工业上电解A的钠盐溶液可以得到多种产物,为防止产物互相反应常使用阳离子交换膜,其阴极反应式为:2H2O+2e-═2OH-+H2↑ | |
| D. | 根据元素周期律,可以推测T元素的单质具有半导体特性,T2W3具有氧化性和还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④③ | B. | ①②④⑤ | C. | ②③④⑤ | D. | ①④③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 定容时观察液面仰视 | B. | 定容时观察液面俯视 | ||
| C. | 有少量NaOH溶液残留在烧杯中 | D. | 容量瓶中原来有少量蒸馏水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只含非极性键的纯净物一定是单质 | B. | 只含极性键的纯净物一定是化合物 | ||
| C. | 离子化合物中一定有离子键 | D. | 纯净物中一定存在化学键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使石蕊变红的溶液中:Na+、K+、AlO2-、HCO3- | |
| B. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=108的溶液中:Mg2+、Cu2+、SO42-、NO3- | |
| C. | 与Al反应能放出H2的溶液中:Fe2+、NH4+、NO3-、SO42- | |
| D. | 0.1 mol•L-1Fe2(SO4)3溶液中:Al3+、Ba2+、Cl-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蔗糖、淀粉、油脂及其水解产物均为非电解质 | |
| B. | 甲烷、乙烯和苯的分子中原子都在同一平面上 | |
| C. | 用食醋可除去热水壶内壁的水垢 | |
| D. | 乙烯和甲烷不能用溴的四氯化碳溶液鉴别 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 碱金属钠、钾保存在煤油中 | |
| B. | 液溴应用水封保存在带橡胶塞的细口瓶中 | |
| C. | 氢氟酸、氯水、AgNO3溶液保存在棕色玻璃瓶中 | |
| D. | 盛Na2SiO3溶液的试剂瓶应用橡胶塞 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com