
某元素的同位素 X,其氯化物XCl2 1.11g配成溶液后,需用1mol/L的AgNO3溶液20mL才能把氯离子完全沉淀下来.已知同位素中有20个中子.
X,其氯化物XCl2 1.11g配成溶液后,需用1mol/L的AgNO3溶液20mL才能把氯离子完全沉淀下来.已知同位素中有20个中子.
(1)计算X的质量数为多少?
(2)指出X元素在周期表中的位置.
考点:
化学方程式的有关计算.
分析:
(1)依据Cl﹣+Ag+═AgCl↓计算Cl﹣的物质的量,从而得出氯化物的物质的量,再利用M=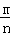 及摩尔质量与相对分子质量的数值相等来计算X的质量数;
及摩尔质量与相对分子质量的数值相等来计算X的质量数;
(2)利用中子数+质子数=质量数,计算质子数,据此写出其在周期表中的位置.
解答:
解:(1)n(AgNO3)=0.02L×1mol•L﹣1=0.02mol,即银离子的物质的量为0.02mol,由Cl﹣+Ag+═AgCl↓可知,硝酸银溶液20mL能把氯离子完全沉淀下来,则Cl﹣的物质的量为0.02mol,XCl2的物质的量为0.01mol,则XCl2的摩尔质量为1.10g 0.01mol=110g/mol,其相对分子质量为110,则X的质量数为110﹣35×2=40;
答:X的质量数为为40;
(2)x的中子数为20,所以X的质子数为40﹣20=20,为钙元素,位于周期表第四周期,第ⅣA族;
答:X元素在第四周期,第ⅣA族.
点评:
本题考查了有关方程式的计算及元素在周期表中位置判断,熟悉发生的反应、原子中质量数、中子数、质子数之间的关系是解题关键,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
若25℃时,CH3COOH的电离平衡常数Ka=1.8×10﹣5,则该温度下0.18mol/L的CH3COONa溶液的pH=9(CH3COONa水解程度很小,计算时可将CH3COO﹣的平衡浓度看成是CH3COONa溶液的浓度)
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y是元素周期表中ⅦA族中的两种元素,下列叙述中能说明X的非金属性比Y强的是( )
|
| A. | X原子的电子层数比Y原子的电子层数多 |
|
| B. | X的氢化物的沸点比Y的氢化物沸点低 |
|
| C. | X的气态氢化物比Y的气态氢化物稳定 |
|
| D. | Y的单质能将X从NaX的溶液中置换出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:
反应X(g)+Y(g)⇌2Z(g);△H<0,达到平衡时,下列说法正确的是()
A. 减小容器体积,平衡向右移动
B. 加入催化剂,Z的产率增大
C. 增大c(X),X的转化率增大
D. 降低温度,Y的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
已建立化学平衡的某可逆反应,当条件改变使化学平衡向正反应方向移动,下列叙述正确的是()
①生成物的质量分数一定增加;②生成物的物质的量一定增加;
③反应物的转化率一定增大;④平衡时反应物的浓度一定降低;
⑤正反应速率一定大于逆反应速率;⑥一定使用了催化剂.
A. ①②⑤ B. ④⑥ C. ②⑤ D. ③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
已知汽车尾气无害化处理反应为2NO(g)+2CO(g)⇌N2(g)+2CO2(g),下列说法不正确的是()
A. 升高温度可使该反应的逆反应速率降低
B. 使用高效催化剂可有效提高正反应速率
C. 反应达到平衡后,NO的反应速率保持恒定
D. 单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
有Xn+、Ym+、Zn﹣,已知它们各自带有的电荷数值m>n,且X、Y、Z三种原子的M电子层中的电子数均为奇数.若按X→Y→Z的顺序,下列说法中正确的是( )
A. 它们的最高价氧化物的相应水化物的碱性依次减弱,酸性依次增强
B. 它们的原子半径依次增大
C. 它们的单质在常温.常压下的密度依次减小
D. 它们的最高价氧化物的水化物都是强电解质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com